Медьорганические соединения
МЕДЬОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ, содержат связь С—Сu. Наиб. изучены производные одновалентной меди CuR, где R-Alk, Ar, R'CH=CH, R'C=C. Они, как правило, представляют собой желтые или красные в-ва полимерного строения. CuAlk не раств. в орг. р-рителях, CuAr и ацети-лениды Сu растворяются в большинстве орг. р-рителей. Наиб. термич. устойчивостью обладают CuCs=CR (в отличие от СuС2 они невзрывчаты), наименьшей - CuAlk, быстро разлагающиеся выше 0°С. CuAr постепенно разлагаются при комнатной т-ре и быстро-при 70-100°С. С введением атома фтора термич. устойчивость медьорганических соединений возрастает. Направление термич. разложения CuR зависит от природы R: если R-Alk, образуются своб. радикалы R. или происходит диспропорционирование на алкен и алкан; если R-Ar или винил, образуются R—R. Вода и протонные к-ты расщепляют CuR с образованием углеводородов. На воздухе
Медьорганические соединения окисляются, при этом CuAlk дают смесь тех же углеводородов, что и при термич. разложении, CuAr-смесь биарилов и фенолов, ацетилениды Cu-димеры соответствующих ацетиленовых соединений. Последняя р-ция применяется в орг. синтезе, причем ацетилениды не выделяются из реакц. смеси (р-ция Глазера):
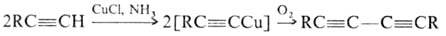
С ацилхлоридами CuR образуют кетоны, с R'Hal-соединения R— R'. Медьорганические соединения реагируют с иодом и бромом:
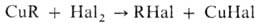
С алифатич. диазосоединениями CuAr взаимод. по схеме:
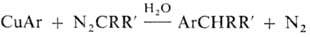
С металлоорг. соед. CuR дают купраты Li[CuR2] и Mg[CuR2]2. Первые благодаря высокой р-римости в эфире и термич. устойчивости находят широкое применение в качестве алкилирующих и арилирующих агентов. В нек-рых случаях они удобнее, чем RLi и RMgX. При окислении кислородом воздуха из купратов с хорошим выходом получают R—R, где R-Ar, RCH=CH или Alk. Купраты гладко присоединяются к алленам и ацетиленам, р-ция протекает региоселективно и стереоспецифично. CuR получают гл. обр. переметаллированием из солей Cu(I) и литий-, магний- или цинкорг. соединений. Перфторалкильные медьорганические соединения образуются при взаимод. перфторалкилиодидов с медной бронзой. Соед. CuC=CR получают р-цией соответствующих ацетиленов с аммиачным р-ром соли Cu(I).
Образование СuС=СН используют для определения ацетилена и его выделения из смесей, для отделения Сu от As, Zn и Cd. Ацетиленид Cu(I) - катализатор полимеризации этилена и пропилена, а также сополимеризации этилена с изобутиленом и 1-бутеном.
Известны также орг. соед. Cu(II) и Cu(III), в частности карбид меди СuС2, а также нек-рые p-комплексы.
Исп. литература для статьи «МЕДЬОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ»: Несмеянов А. Н., в кн.: Методы элементоорганической химии. Подгруппы меди, скандия, титана, ванадия, хрома, марганца. Лантаноиды и актиноиды, кн. 1, М., 1974, с. 11-60; Jukes A. E., в кн.: Advances in organo-metallic chemistry, v. 12, N. Y., 1974, p. 215-322. O.A. Птицына.
