Олова галогениды
ОЛОВА ГАЛОГЕНИДЫ. Известны простые ди- и тетра-галогениды SnX2 и SnX4 (см. табл.), смешанные галогениды 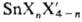 , оксогалогениды, а также комплексные - галогено-станнаты. 8пС14-бесцв. жидкость, остальные - кристаллы; хлориды и фториды Sn, а также SnBr4 бесцветны. Тетра-галогениды - к-ты Льюиса, по силе их можно расположить в ряд SnCl4 " SnBr4 > SnI4. Наиб. практич. значение имеют хлориды Sn.
, оксогалогениды, а также комплексные - галогено-станнаты. 8пС14-бесцв. жидкость, остальные - кристаллы; хлориды и фториды Sn, а также SnBr4 бесцветны. Тетра-галогениды - к-ты Льюиса, по силе их можно расположить в ряд SnCl4 " SnBr4 > SnI4. Наиб. практич. значение имеют хлориды Sn.
Тетрахлорид SnCl4 дымит на воздухе вследствие гидролиза; tкрит 318,7°С, pкрит 3,7 МПа; ур-ние температурной зависимости давления пара: lg р(Па) = 12,87-1925/T (298-388 К). Хорошо смешивается с водой, при этом объем р-ра заметно меньше суммы объемов компонентов. Из горячих конц. водных р-ров при охлаждении до 83-63°С выделяется тригидрат, при 63-56 °С-тетрагидрат, при 56-19°С-пентагидрат, ниже 19°С-октагидрат. Разб. р-ры SnCl4 гидролизуются, в р-рах образуется также Н2 [SnCl6].
СВОЙСТВА ГАЛОГЕНИДОВ ОЛОВА
| Показатель | SnF4 | SnCl4 | SnBr4 | SnI4 | | SnCl2, | SnBr, | SnI2, | ||
| Сингония | Тетрагон. | | Моноклинная | Кубич. | Моноклинная | Ромбич. | Ромбич. | Моноклинная | ||
| Параметры элементарной ячейки: | | | | | | | | | ||
| а, нм | 0,4048 | - | 1,059 | 1,225 | 1,346 | 0,779 | - | 1,429 | ||
| b, нм | - | - | 0,710 | - | 0,492 | 0,921 | - | 0,453 | ||
| с, нм | 0,793 | - | 1,066 | - | 1,386 | 0,443 | - | 1,072 | ||
| угол, град | _ | _ | 103,9 | _ | 109,5 | _ | _ | 92 | ||
| Пространств. группа | I4/ттт | _ | P21/c | Pa3 | P21/c | Рhaт | _ | Cm | ||
| Число формульных единиц в ячейке | 2 | _ | | 8 | 16 | 4 | _ | 6 | ||
| Т. кип., оС | 705* | 114 | 202 | 364,5 | 853 | 652 | 620 | 717 | ||
| Т.пл., °С | _ | -33 | 31 | 144,5 | 215,0 | 246 | 215,5 | 320 | ||
| Плотн., г/см3 | 4,78 | 2,23 | 3,34 (35 °С) | 4,5 | 4,87** | 3,95 | 5,12 | 5,19 | ||
| | | 165,3 | | 85,0 | 72,4 | 78,0 | | | ||
| | - | -528,8 | -405,8 | - | -650 | -333 | -260 | -145,2 | ||
| | - | 258,5 | 264,7 | - | 96,2 | 134,0 | - | - | ||
* Т-ра возгонки. ** Плотн.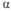 -SnF2 5,33 г/см3.
-SnF2 5,33 г/см3.
Тетрахлорид раств. в этаноле, диэтиловом эфире и нек-рых др. орг. р-рителях; растворяет S, Р, галогены; с Сl2 дает эвтектику при -106°С, содержащую 86% хлора. Хлориды Fe, Al, Та, Nb частично раств. в SnCl4. Тетрахлорид - окислитель; склонен к р-циям присоединения, легко образует комплексные соед. с НСl, NH3, PCl5. Так, из смеси р-ров SnCl4 и NH4Cl кристаллизуется гексахлоростаннат (NH4)2 [SnCl6], к-рый возгоняется при 400 °С. Гексахлоро-станнаты щелочных металлов разлагаются выше 600 °С. Известны аддукты SnCl4·NO, 3SnCl4·2PH3, продукты присоединения спиртов, орг. сульфидов, аром, соед., эфиров и др. Получают SnCl4 взаимод. Sn с Сl2 (сильноэкзотермич. р-ция). Применяют для получения Sn и оловоорг. соед., как катализатор полимеризации и др. р-ций, протраву при крашении тканей, для утяжеления натурального шелка, как компонент светочувствит. бумаги, для отделения Rb и Cs от К в аналит. химии.
Дихлорид SnCl2 в парах при 600-700°С димерен; ур-ние температурной зависимости давления пара lg р (Па) = = 12,73-4480/T (677-902 К); р-римость в воде 83,8 г в 100 г при О °С. Из водного р-ра кристаллизуется дигидрат, в разб. водных р-рах гидролизуется. В присут. небольших кол-в НСl р-римость SnCl2 в воде уменьшается, но при высокой кислотности повышается. SnCl2 хорошо раств. в этаноле, диэтиловом эфире, ацетоне, пиридине и др. орг. р-рителях; р-ры SnCl2-сильные восстановители. Хлор окисляет SnCl2 до SnCl4, О2-до оксохлорида. С аммиаком SnCl2 образует аммиакаты SnCl2·nNH3 (n = 1, 4, 9), с хлоридами металлов-комплексные соед., напр. K[Sn2Cl5] (т. пл. 218 °С), К [SnCl3] (т. пл. 255 °С), Sn [Аl2Сl8] (т. пл. 209 °С), Sn [A1C15] (т. пл. 158,5СС), Sn[Ta2Cl12] (т. пл. 239 °С). Получают SnCl2 взаимод. Sn с Сl2, НСl или хлоридами др. металлов. Применяют как катализатор полимеризации эпоксидов, восстановитель в орг. синтезе, протраву при крашении тканей, для обработки пов-сти стекла и пластмасс перед металлизацией для повышения адгезии, как компонент флюса при сварке, для получения Sn, как реагент для определения Сl2, I,, Hg2+, Fe3 + и др., для обесцвечивания нефтяных масел. Тетрафторид SnF4 хорошо раств. в холодной воде, не раств. в большинстве орг. р-рителей, раств. в горячем ТГФ. Образует гексафторостаннаты щелочных металлов M2[SnF6], а также (NH4)4 [SnF8], K3H[SnF8] и др. Получают SnF4 либо фторированием SnCl4, либо прямым взаимод. Sn и F2. Дифторид SnF2 кристаллизуется в ромбич. (a) и моноклинной (b) модификациях, хорошо раств. в воде, этаноле, диэтиловом эфире, практически не раств. в СНСl3; с фторидами щелочных металлов и аммония образует соед. М [SnF3], известен также Na [Sn2F5]; получают взаимод. SnO с газообразным HF. Применяют как компонент зубных паст, флюсов для пайки, твердых электролитов и электролитов для лужения.
Тетрабромид SnBr4 и тетраиодид SnI4 получают взаимод. Sn соотв. с Вг2 и I2. Из водного р-ра при обычной т-ре SnBr4 кристаллизуется в виде тетрагидрата. Гексабро-мооловянная к-та Н2 [SnBr6]·8Н2О-бесцв. расплывающиеся на воздухе кристаллы; известны гексабромостаннаты (IV) М2 [SnBr6]. Тетраиодид образует сильно светопреломляю-щие кристаллы, окрашенные от желтого до желто-коричневого цвета; раств. в CS2, этаноле, диэтиловом эфире, бензоле и др. орг. р-рителях; гидролизуется водой, поэтому иодостаннаты нельзя получить из водного р-ра. Дибромид SnBr2-желтые кристаллы; хорошо раств. в воде, в р-рах гидролизуется. Дииодид SnI2-оранжево-красные кристаллы, слабо раств. в воде. SnI2 и SnBr2 раств. в метаноле; по хим. св-вам сходны с SnCl2 и образуют аналогичные комплексные соединения.
Получены смешанные галогениды: SnBr3Cl (т. пл. 1,0°С, т. кип. 73 °С, плотн. 3,12 г/см3), SnBrCl3 (т. пл. -1,0°С, т. кип. 50 °С, плотн. 2,51 г/см3) и др.
Лит.: Фурман А. А., Неорганические хлориды (Химия и технология), М., 1980. См. также лит. при ст. Олово. Н.П. Дергачева.

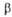 -SnF,
-SnF,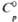 , Дж/(моль·К).
, Дж/(моль·К).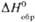 , кДж/моль
, кДж/моль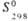 , Дж/(моль·К)
, Дж/(моль·К)