Электромиграционные методы
ЭЛЕКТРОМИГРАЦИОННЫЕ МЕТОДЫ, методы исследования в р-рах ионизир. в-в и разделения их сложных смесей; основаны на явлении переноса заряженных частиц в электрич. поле, приложенном к изучаемому р-ру (см. также Электрокинетические явления).
Осн. параметр, характеризующий перенос частиц,- подвижность и, т. е. расстояние l, нак-рое в-во переместится под действием единицы градиента электрич. потенциала Е за единицу времени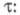
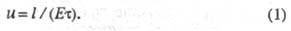
Процессы, связанные с комплексообразованием, ассоциацией или пересольватацией ионов, а также с изменением состояния р-рителя, приводят к изменению заряда либо радиуса ионов, что оказывает влияние на их подвижность; на этом основано применение электромиграционных методов для исследования р-ций в р-рах.
Неодинаковая подвижность мол. ионов и заряженных частиц разл. хим. природы позволяет использовать электромиграционные методы также для разделения смесей; в данном случае эти методы часто наз. электрофорезом.
Методы измерения подвижности заряженных частиц. Подвижность, или скорость миграции индивидуальных ионов, можно определять: 1) по изменению концентрации ионов исследуемого элемента в приэлектродном пространстве при электролизе; 2) путем смещения в электрич. поле узких зон изучаемых ионов; 3) с помощью подвижной границы между зонами (фронтальные методы, изотахофорез).
Исследование реакций в растворах. Информацию о равновесных процессах в р-ре получают при изучении зависимости скорости миграции ионов исследуемого элемента от концентрации одного или неск. участвующих в р-ции в-в. По этой зависимости можно выявлять состав продуктов р-ции и определять константы равновесия.
В случае р-ций комплексообразования изучаемый металл М может находиться одновременно в неск. ионных формах связи с лигандом А, между к-рыми устанавливается подвижное равновесие. В такой системе общее, или суммарное, перемещение в электрич. поле всех ионов, содержащих М и имеющих индивидуальные подвижности иi, происходит с нек-рой ср. скоростью ис, характеризующей суммарный электромиграц. перенос металла в единицу времени:
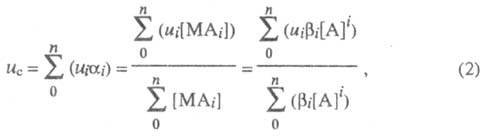
где i - число лигандов в комплексе;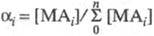 - доля металла, связанного в i-ую ионную форму;
- доля металла, связанного в i-ую ионную форму;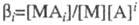 - полная константа устойчивости ионной формы; [М], [А] и [МАi] - соотв. равновесные концентрации металла, лиганда и комплекса.
- полная константа устойчивости ионной формы; [М], [А] и [МАi] - соотв. равновесные концентрации металла, лиганда и комплекса.
Кривая электромиграции (рис. 1), отражающая смещение подвижного равновесия между разл. ионными формами при изменении равновесной концентрации лиганда, устанавливает области существования: своб. ионов (I); координационно ненасыщенных форм (II); координационно насыщенных комплексных ионов (III).
Состав комплексных ионов можно определять неск. приемами: по эмпи-рич. зависимости между подвижностью ионов и величиной их заряда; из соотношения общей и равновесной концентраций лиганда, к-рое определяется по скорости электромиграции введенного в систему вспомогат. металла (по ур-нию 2); по соотношению между коэф. диффузии и подвижностью при одной и той же концентрации лиганда. Константы устойчивости ионных форм рассчитывают путем решения системы из п ур-ний вида (2), где п равно числу ионных форм.
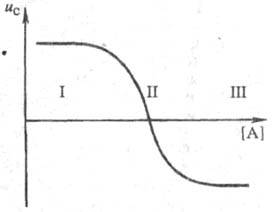
Рис. 1. Зависимость средней скорости миграции металла ис от концентрации лиганда [А]: I, II, Ш - области осуществления соотв. своб. ионов металла, координационно ненасыщенных форм и координационно насыщенных комплексных ионов.
При исследовании хим. взаимодействий в р-ре важно сохранение постоянства состава фонового электролита, к-рое может нарушаться вследствие электродных р-ций. Поэтому целесообразно использовать аппаратуру, предотвращающую проникновение продуктов электролиза в рабочую часть прибора. Если это условие выполнено, то электромиграционные методы дают достаточно правильные результаты благодаря тому, что отсутствует необходимость введения в изучаемую систему новых фаз - ионообменных смол, экстрагентов и т. п., вызывающих побочные равновесные процессы.
Помимо равновесий электромиграционные методы позволяют исследовать кинетику комплексообразования, используя явление дополнит. квазидиффузионного размывания под действием электрич. поля первоначально узкой зоны, содержащей разл. ионные формы с разными знаками заряда. Для достижения этого эффекта необходимо приложить поле такой напряженности, чтобы скорость электромиграц. переноса ионов превышала скорость протекания комплексообразования.
Для изучения кинетики р-ций можно использовать также зонную электромиграцию ионов в неравновесном с ними электролите. В обоих случаях применение электромиграционных методов целесообразно при анализе процессов, скорость к-рых лежит в пограничной области между медленными и быстрыми р-циями.
Закономерности электромиграции ионов в расплавах солей исследованы в значительно меньшей степени, чем в водных р-рах. Обычная среда при проведении электромиграции в расплавленных солях - безводные расплавы нитратов и перхлоратов щелочных металлов или эвтектич. смеси, имеющие сравнительно низкую т-ру плавления.
Для электромиграции в расплавах характерны две осн. проблемы: сильное взаимод. ионов изучаемых металлов и расплавленной соли; отсутствие электрически нейтрального р-рителя, для к-рого можно измерить истинную скорость движения ионов. Поэтому обычно их подвижность определяют относительно прибора, в к-ром проводят электромиграцию. В этом случае данные о подвижности в расплавах смещены на неизвестную постоянную величину.
Разделение смесей. Различают след. методы электромиграц. разделения смесей: зонный электрофорез; фокусирующий ионный обмен; фронтальные методы; изотахофорез.
Зонный электрофорез чаще всего реализуют в среде пористого наполнителя, пропитанного р-ром электролита. Разделяемая смесь должна быть первоначально сосредоточена в узкой зоне, имеющей относительно малые линейные размеры. Благодаря устранению конвективных потоков жидкости зоны исследуемых элементов по окончании опытов сохраняют достаточно четкие границы. В качестве наполнителей обычно используют хроматографич. и фильтровальную бумаги, порошки (напр., кварцевый песок), разл. гели (напр., крахмала). При проведении миграции в пористой среде возможно влияние дополнит. факторов адсорбции мигрирующих ионов на пов-сти среды, электроосмотич. потока жидкости, обусловленного поверхностным зарядом наполнителя, а также размытием зоны мигрирующего в-ва.
В водных р-рах сильных электролитов, не взаимод. с разделяемыми в-вами, подвижности ионов мн. элементов из-за сильной гидратации имеют близкие значения, что делает разделение недостаточно эффективным. В р-рах комплексообразующих в-в неодинаковая устойчивость комплексных ионов разделяемых элементов приводит к различию соотношения концентраций ионных форм и, следовательно, суммарных скоростей миграции элементов [см. ур-ние (2)]. Однако эти различия могут наблюдаться лишь в довольно узкой зоне концентраций лиганда или значений рН (рис. 2). Применяют неск. вариантов зонного электрофореза.
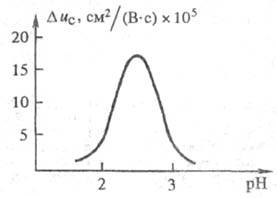
Рис. 2. Зависимость разности средних скоростей миграции La и Се от рН 0,01 %-ного р-ра этилендиаминтетраукеуснойк-ты.
Электрофорез на бумаге осуществляется на листах (полосках) хроматографич. или фильтровальной бумаги, концы к-рой опущены в электродные камеры. Разделяемая смесь наносится на бумагу в виде пятна либо узкой зоны. По способу отведения теплоты, выделяющейся при прохождении через бумагу электрич. тока, используют приборы: с охлаждающими пластинами из изолирующих материалов; с охлаждающей несмешивающейся с водой орг. жидкостью (рис. 3), напр. керосином; с естеств. охлаждением бумаги на воздухе или во влажной камере.
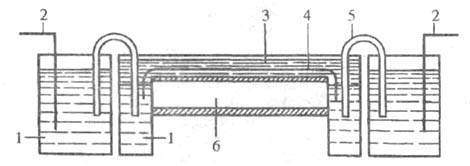
Рис. 3. Схема прибора для электрофореза на бумаге: 1 - буферный электролит; 2 - электроды; 3 - кювета с охлаждающей орг. жидкостью; 4 - полоска хроматографич. бумаги; 5 - электролитич. мостик; 6 - водяная рубашка.
При разделении радиоактивных ионов пористой средой служат пленки ацетилцеллюлозы, обладающие однородной микропористой структурой.
Тонкослойный электрофорез. Электромиграцию проводят в слоях порошкообразных материалов (целлюлоза, ацетилцеллоза, А12О3, кварцевый песок и др.).
Электрофорез в гелях- применяют гл. обр. для разделения высокомол. соед., напр. белков. Для этого обычно в виде блоков и колонок используют гели крахмала и полиакриламида. Адсорбция разделяемых в-в и электроосмос в этих материалах незначительны.
Капиллярный электрофорез- осуществляют в заполненных буферным р-ром стеклянных или кварцевых капиллярах длиной 40-100 см и сечением 50-200 мкм. При напряженности электрич. поля 200-500 В/см разделение биол. объектов достигается за 1-2 мин.
Непрерывный электрофорез. Электрич. поле Е направлено под прямым углом к направлению движения жидкости, протекающей через пористую среду. Разделяемая смесь (напр., компонентов А и Б) подается узкой струей (рис. 4). Результирующая траектория движения заряженных частиц представляет собой прямую, тангенс угла наклона к-рой равен отношению скорости миграции частиц к скорости прохождения электролита. Стабилизирующими материалами могут служить указанные выше пористые среды.
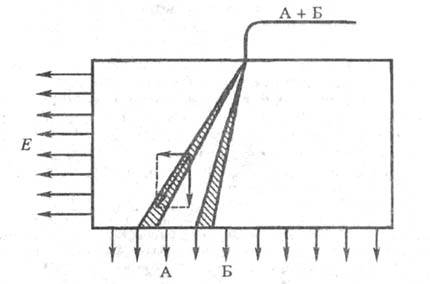
Рис. 4. Схема непрерывного электрофореза.
Фокусирующий ионный обмен. Этот метод часто наз. электрофоретич. фокусировкой или просто электрофокусированием, связан с наложением градиента концентрации или рН р-ра параллельно электрич. полю. Благодаря этому разделяемые ионы могут изменять величину и знак заряда по мере перемещения в поле градиента. При этом в фиксир. точках системы каждый компонент переходит в изоэлектрич. состояние, в к-ром ср. заряд частиц данного компонента равен нулю. Упомянутые точки являются местом концентрирования (фокусирования) отдельных компонентов смеси (рис. 5). Положение зон фокусирования определяется градиентом концентрации комплексообразующего реагента или рН р-ра и константами устойчивости комплексных ионов разделяемых элементов. При разделении смеси белков или др. амфотерных соед. положение зон определяется значениями их изоэлектрич. точек.
Для создания градиента рН электродные камеры заполняются буферными р-рами с разными значениями рН. Напр., для разделения редкоземельных элементов цериевой группы в 0,001 М р-ре этилендиаминтетрауксусной к-ты рН должен изменяться по длине колонки от 1,7 у анода до 2,4 у катода.
В сер. 60-х гг. 20 в. было предложено создавать градиент рН с помощью амфолитов - смесей алифатич. полиаминокислот. Под влиянием электрич. поля амфолиты распределяются в соответствии со своими изоэлекгрич. точками и тем самым образуют градиент рН. Применение амфолитов позволяет добиться весьма высокой разрешающей способности метода: в нек-рых случаях удается разделить белки, изоэлектрич. точки к-рых различаются на 0,02 единицы рН.
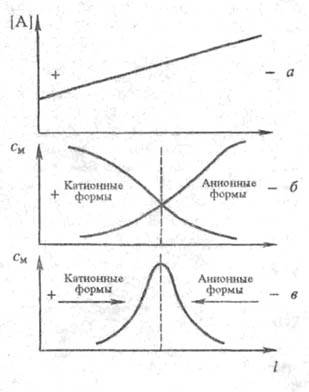
Рис. 5. Схема, поясняющая метод электрофокусирования: а - образование градиента концентрации лиганда [А]; б - распределение ионных форм мигранта; в - кон-центрирование лиганда в узкой зоне; см - концентрация мигранта.
Описанный метод, являясь самостоятельным, в то же время представляет собой вариант зонного электрофореза. Во всех модификациях последнего идентификацию и количеств. определение в-в в зонах можно проводить как непосредственно на носителе, так и после элюирования. В обоих случаях используют методы радиоактивных индикаторов, фотометрию в прямом и отраженном свете, люминесцентный анализ.
Фронтальные методы основаны на измерении скорости перемещения границы раздела р-ров с разной плотностью. Классич. вариант метода был разработан в 1930 и с тех пор применяется для определения подвижности и разделения высокомол. в-в, в частности белков. В простейшей модификации метода в U-образную трубку помещают р-р белков, а над ним буферный электролит, в к-рый погружены электроды. При наложении электрич. поля индивидуальные белки перемещаются с разл. скоростями, образуя серию границ. Их положение регистрируют оптич. методами по изменению коэф. преломления.
Изотахофорез. Осн. частью прибора служит капиллярная трубка с анодным и катодным резервуарами на концах. При анализе анионов анодное отделение и капилляр заполняют т. наз. лидирующим электролитом, содержащим анион с высокой подвижностью. Ср. скорость миграции анионов в этом электролите должна быть выше подвижности любого аниона в исследуемой смеси. Катодное отделение заполняют т. наз. замыкающим электролитом, анион к-рого имеет подвижность меньшую, чем подвижность любого др. аниона в смеси. Анализируемый образец, в к-ром нужно определить содержание анионов, вносят между предшествующим и замыкающим электролитами. После подачи напряжения (5-10 кВ) при силе тока до 100 мкА по мере движения анионов к катоду постепенно образуются зоны индивидуальных анионов определенной длины, разделенные четкими границами, ширина к-рых составляет 0,2-0,3 мм при диаметре капилляра 0,1 мм. После этого все зоны будут перемещаться с одинаковой скоростью (отсюда назв. метода). Соотношение концентраций анионов в двух соседних зонах с1 и с2 в установившемся режиме будет определяться выражением Кольрауша:
с1/с2 = n1/n2, (4)
где n1и n2 - числа переноса.
При анализе катионов лидирующий электролит должен содержать катионы с высокой подвижностью, замыкающий -с миним. для данной системы скоростью миграции.
Кол-во в-ва в зоне Q и ее длина l в капилляре постоянного сечения S связаны простым соотношением:
Q = ClS, (5)
где С - коэф. пропорциональности.
В установившеся режиме градиент потенциала при переходе от лидирующего к замыкающему электролитам скачкообразно возрастает в соответствии с подвижностью ионов, составляющих данную зону. Это приводит к температурным скачкам между зонами, регистрируя к-рые с помощью термопары можно определить расстояние между зонами и по выражению (5) найти кол-во в-ва в зоне.
Применение. Электромиграционные методы широко используют при анализе биол. образцов, получении чистых препаратов, для диагностики в медицине. В неорг. анализе электромиграционные методы применяют для разделения смесей радиоактивных элементов, а также в качестве метода физ.-хим. исследования.
Лит.: Троицкий Г. В., Электрофорез белков, Хар., 1962; Константинов Б.В., Ошуркова О. В., "Ж. технич. физики", 1966, т. 36, № 5, с. 942-57; Духин С. С, Дерягин Б. В., Электрофорез, М., 1976; Макарова Т. П., Степанов А. В., "Радиохимия", 1977, т. 19, № 2, с. 125-46; Степанов А.В., Корчемная Е. К., Электромиграционный метод в неорганическом анализе, М., 1979; Остерман Л. А., Исследование биологических макромолекул электрофокусированием, иммуноэлектрофорезом и радиоизотопными методами, М., 1983; Schumacher E., "Helv. Chim. Acta", 1957, v. 40, fasc. 1, p. 221-28; Shaw D. J., Electrophorcsis, L.-N. Y., 1969; Everaerts P.M., "J. Chromatogr.", 1972, v. 65, p. 3-17; Mason C., "Lab. Equip. Dig.", 1990, v. 1, p. 221.
А. В. Степанов.
