Вещества, экстрагируемые органическими растворителями из подщелоченных водных вытяжек
В химико-токсикологическом анализе наиболее многочисленную группу токсических соединений составляют вещества, которые экстрагируются органическими растворителями из подщелоченных водных вытяжек. Ниже приводится описание свойств, применения и методов анализа только некоторых из этих веществ, которые неоднократно были причиной отравлений.
К числу рассматриваемых ниже веществ относятся алкалоиды, синтетические соединения, полученные на основе алкалоидов, и ряд других препаратов.
Включенные в этот раздел алкалоиды являются производными хинолина (хинин), изохинолина (морфин, кодеин, папаверин, галантамин), пиридина (анабазин, никотин, ареколин), пиперидина (кониин), тропана (атропин, скополамин, кокаин), индола (стрихнин, бруцин, резерпин) и др.
В этот раздел книги включены синтетические вещества, полученные на основе морфина (апоморфин, дионин, героин), препараты, являющиеся производными фенотиазина (аминазин, ди-празин и др.), бензодиазепина (хлордиазепоксид, диазепам, нитразепам), анилина (новокаин и дикаин) и др.
Обнаружение приведенных выше токсических веществ производят в хлороформных вытяжках из подщелоченных водных вытяжек. Для этой цели также могут быть использованы сухие остатки, полученные после выпаривания хлороформных вытяжек, или растворы сухих остатков.
§ 32. ХИНИН
Хинин является алкалоидом, содержащимся в коре различных видов хинного дерева. В этой коре кроме хинина содержится хинидин, цинхонин, цинхонидин и ряд других алкалоидов. В состав молекулы хинина входят хинолиновый и хинуклидиновый циклы, связанные группой атомов — СН — ОН. Хинин является изомером хинидина. В медицинской практике применяются гидрохлорид, дигидрохлорид и сульфат хинина. Основание хинина растворяется в этиловом спирте (1:1), хлороформе (1 : 3), диэтиловом эфире, насыщенном водой (1 :4), слабо растворяется в воде. Гидрохлорид хинина растворяется в этиловом спирте (1:1), хлороформе (1:2), воде (1 : 23), слабо растворяется в диэтиловом эфире. Сульфат хинина растворяется в этиловом спирте (1 :95), слабо растворяется в воде (1 : 810), диэтиловом эфире и хлороформе.
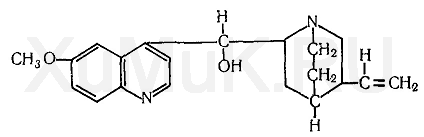
Хинин экстрагируется органическими растворителями из щелочных водных растворов. Максимальные количества хинина экстрагируются хлороформом при рН = 9...10.
Применение. Действие на организм. В зависимости от принятой дозы хинина он может вызывать угнетение центральной нервной системы, головную боль, головокружение, нарушение зрения. Хинин возбуждает мускулатуру матки и усиливает ее сокращение. Он так же вызывает сокращение селезенки. Хинин действует на возбудителя малярии и является одним из эффективных противомалярийных лекарственных препаратов. Его применяют при аритмиях. Хинин применяется в акушерской практике для возбуждения и усиления родовой деятельности. При передозировке хинина, применяемого беременными женщинами, может наступить аборт.
Метаболизм. В организме хинин подвергается метаболизму путем окисления хинолинового и хинуклидинового циклов. При этом образуются 2-оксихинин, 2'-оксихинин, диоксихинин. При метаболизме может окисляться винильная группа в молекуле хинина с образованием хинетина. Также может окисляться хинуклидиновый цикл с образованием гемохинной кислоты (6-метокси-хинолин-4-кетокарбоновой кислоты). Метаболиты и незначительная часть несвязанного хинина выводится из организма с мочой.
Обнаружение хинина
Предварительная проба на наличие хинина в моче. В делительную воронку вносят 2 мл мочи, которую подщелачивают раствором аммиака, а затем прибавляют 4 мл хлороформа и взбалтывают в течение 5 мин. От водной фазы отделяют слой органического растворителя, который взбалтывают с 3 мл 10 %-го раствора серной кислоты. Синяя флуоресценция водной фазы указывает на наличие хинина в моче. Флуоресценция становится более выраженной, если кислую водную вытяжку облучать УФ-светом.
Реакции с реактивами группового осаждения алкалоидов. Хинин дает осадки с реактивами Бушарда, Драгендорфа, Майера, Зонненшейна и другими реактивами группового осаждения алкалоидов.
Обнаружение хинина по флуоресценции. Растворы хинина, подкисленные серной кислотой, имеют голубую флуоресценцию. При наличии ионов хлора и некоторых других ионов в растворах флуоресценция хинина ослабляется.
Флуоресценция хинина как двухосновного основания зависит от рН среды. В кислой среде хинин имеет голубую флуоресценцию. В щелочной среде (рН~9) хинин имеет фиолетовую флуоресценцию. Продукты окисления хинина имеют желто-зеленую флуоресценцию.
Выполнение опыта. Исследуемый раствор вносят в фарфоровую чашку и выпаривают досуха. К сухому остатку прибавляют 4—5 мл 0,1 н. раствора серной кислоты. Полученный раствор переносят в пробирку, которую облучают УФ-лучами. При наличии хинина появляется голубая флуоресценция раствора. От прибавления к этой жидкости нескольких капель 0,1 н. раствора гидроксида натрия интенсивность голубой флуоресценции ослабевает, а затем (при рН~9) появляется фиолетовая флуоресценция.
Если к раствору хинина, подкисленному серной кислотой, прибавить несколько капель бромной воды, разбавленной десятикратным объемом воды (до полного тушения флуоресценции), а затем прибавить несколько капель 25 %-го раствора аммиака до щелочной реакции, то появляется желто-зеленая флуоресценция.
Талейохинная реакция. От прибавления к хинину бромной воды, а затем аммиака образуется зеленого цвета талейохин, который экстрагируется хлороформом:
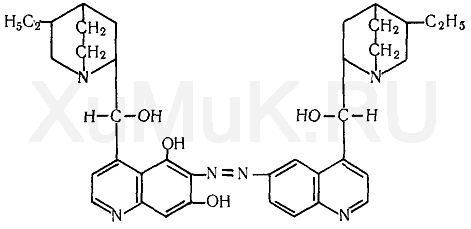
Выполнение реакции. Раствор исследуемого вещества выпаривают досуха. К сухому остатку прибавляют 1 мл воды. К полученному раствору по каплям прибавляют бромную воду (избегая ее избытка) до слабо-желтой окраски. От прибавления нескольких капель раствора аммиака к слабо-желтому раствору появляется ярко-зеленая окраска, которая при нейтральной реакции становится синей, а при добавлении кислоты переходит в красную или фиолетовую. При взбалтывании жидкости, имеющей зеленую окраску, с хлороформом последний приобретает зеленую окраску.
На воспроизводимость реакции влияет концентрация исследуемого вещества, объемы прибавляемых реактивов и т. д. Реакции мешают амидопирин, антипирин, кофеин и др.
Эритрохинная реакция. Несколько капель исследуемого раствора выпаривают досуха, прибавляют 1 мл воды, слабо подкисленной серной или уксусной кислотой, каплю бромной воды и каплю 10%-го раствора гексацианоферрата (III) калия. Полученную жидкость хорошо взбалтывают, затем по каплям прибавляют аммиак до щелочной реакции. При наличии хинина в исследуемом растворе появляется розовая или красно-фиолетовая окраска, которая при взбалтывании с хлороформом переходит в хлороформный слой.
Обнаружение хинина методом хроматографии. Для обнаружения хинина применяют метод хроматографии в тонком слое силикагеля. С этой целью используется та же методика, что и для обнаружения морфина (см. гл. V, § 34).
Пятна хинина на хроматограмме имеют розовато-бурую окраску (Rf = 0,39±0,01).
Обнаружение хинина по УФ- и ИК-спектрам. Основание хинина в этиловом спирте имеет максимумы поглощения при 236, 278 и 332 нм, а хинин в 0,1 н. растворе серной кислоты имеет максимумы поглощения при 250, 316 и 346 нм. В ИК-области спектра основание хинина (диск с бромидом калия) имеет основные пики при 1235, 1510, 1030 и 1619 см -1.


