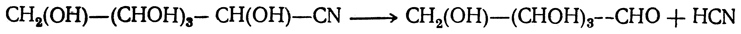Способы получения оксиальдегидов, оксикетонов и моносахаридов
1. Окисление многоатомных спиртов. Например, окислением этиленгликоля СН2ОН—СН2ОН может быть получен простейший оксиальдегид СН2ОН—СНО, обычно называемый гликолевым альдегидом. Окислением глицерина могут быть получены оксиальдегид и оксикетон:

Окислением высших многоатомных спиртов могут получаться моносахариды, как альдозы, так и кетозы. Например, при окислении маннита получаются альдогексоза и кетогексоза:

Интересно, что превращение многоатомных спиртов в кетозы может быть осуществлено путем биологического окисления, например с помощью энзима, вырабатываемого так называемой сорбозной бактерией.
2. Обмен галоидов на гидроксилы в галоидных производных альдегидов и кетонов. Например:
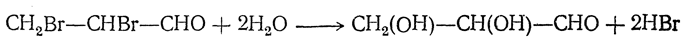
3. Конденсация альдегидов, кетонов или альдегидов с кетонами. Конденсацией двух молекул ацетальдегида получается альдоль СН3—СН(ОН)—СН2—СНО, являющийся одним из простейших представителей β-оксиальдегидов; конденсацией двух молекул ацетона получается оксикетон — диацетоновый алкоголь (СН3)2С(ОН)—СН2—СО—СН3 и т. д. Конденсацией муравьиного альдегида под действием известковой или баритовой воды получается смесь оксиальдегидов и оксикетонов, в которой содержатся также и гексозы.
Этим способом А. М. Бутлеров еще в 1861 г. получил густой сироп, в котором он установил присутствие сахаристого вещества, названного им метиленитаном. Им же была отмечена важность этого первого искусственного синтеза вещества, относящегося к классу углеводов. Впоследствии Э. Фишер из такого сиропа, содержащего смесь гексоз, выделил гексозу СбН12О6, названную им акрозой. Она оптически недеятельна, как и все синтетические вещества. Э. Фишер доказал, что акроза представляет собой рацемическую смесь антиподов кетозы СН2ОН—(СНОН)3—СО—СН2ОН, а именно: природной D-фруктозы и ее не встречающегося в природе антипода — L-фруктозы.
Реакция конденсации формальдегида в акрозу выражается суммарным уравнением
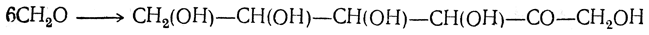
Как было позднее показано, эта реакция протекает, вероятно, последовательно через стадии образования промежуточных соединений с участием меньшего числа молекул формальдегида. Так, при конденсации формальдегида под действием углекислого кальция в числе прочих продуктов получается гликолевый альдегид, образовавшийся путем альдольной конденсации двух молекул муравьиного альдегида:
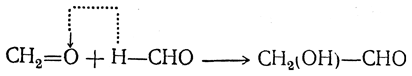
Высшие моносахариды могут быть получены также конденсацией низших оксиальдегидов. Так, конденсацией двух или трех молекул гликолевого альдегида получены тетроза и гексоза:
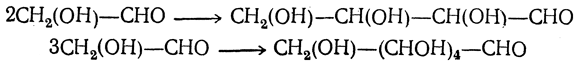
Синтез моносахаридов из альдегидов и кетонов путем альдольной конденсации играет важную роль в биологических процессах.
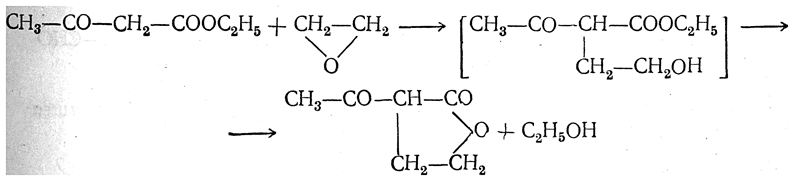
4. Конденсация натрийацетоуксусного эфира с окисью этилена. Таким путем может быть легко получен γ-ацетопропиловый спирт, или 4-кетопентан-1-ол (И. Л. Кнуньянц, Г. В. Челинцев, Е. Д. Осетрова). Схематически процесс можно представить так:
Образующийся лактон расщепляют затем разбавленными кислотами:
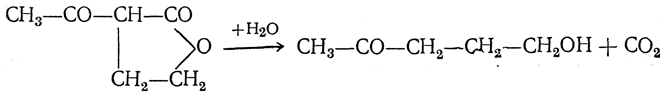
5. Гидролиз полисахаридов и гликозидов. Моносахариды часто получаются при процессах присоединения воды (гидролиз) к полисахаридам и гликозидам.
6. Восстановление альдоновых кислот. Альдозы могут быть получены восстановлением соответствующих одноосновных многоатомных оксикислот, так называемых альдоновых кислот. Легко восстанавливаются (например, амальгамой натрия) не самые оксикислоты, а их лактоны. Например, альдогексозы легко получаются восстановлением лактонов соответствующих гексоновых кислот.
Эта реакция позволяет переходить от низших моносахаридов к высшим. Так, в результате присоединения синильной кислоты, например, к глюкозе получается нитрил СН2(ОН)—(СНОН)4—СН(ОН)—CN, который при омылении дает глюкогептоновую кислоту; при восстановлении лактона этой кислоты получается альдогептоза. Этим способом Э. Фишеру удалось дойти до синтеза ноноз.
7. Расщепление соединений с бóльшим числом атомов углерода в молекуле. Чрезвычайно важными способами получения оксиальдегидов, и в частности моноз, являются способы, при которых происходит расщепление углеродной цепи. Пользуясь ими, можно осуществить последовательный переход от высших моноз к низшим.
Так, окислением альдоновых кислот перекисью водорода в присутствии ацетата окисного железа можно получить монозу с меньшим на единицу числом атомов углерода в молекуле, например:
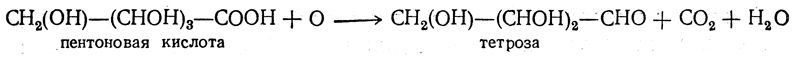
Подобный же переход осуществляется при действии на амиды альдоновых кислот солями хлорноватистой кислоты (в щелочной среде), например:
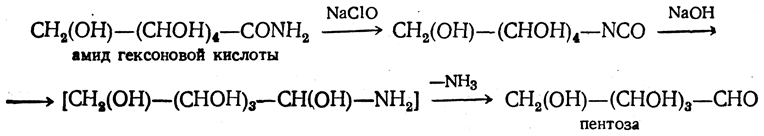
Наконец, оксимы гексоз при действии уксусного ангидрида могут отщеплять молекулу воды, образуя нитрилы глюконовых кислот:
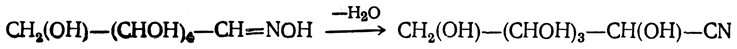
Последние при действии аммиачного раствора окиси серебра отщепляют молекулу синильной кислоты, образуя низшие монозы: