Метан, этан, пропан, бутан и изобутан - физичесике и химические свойста
Метан СН4
называется также болотным газом, так как он составляет главную часть горючих газов, пузырьками поднимающихся из болотной тины, где метан образуется при гниении растительных остаткоз (целлюлозы) без доступа воздуха. Кроме того, его называют рудничным газом, так как он образуется при медленном разложении каменного угля под землей и иногда выделяется в большом количестве в рудниках; образование смесей метана с воздухом может служить причиной опасных взрывов. Большие количества метана содержатся в растворенном состоянии в нефти; в нефтеносных местностях он иногда выделяется из земли. Метан входит также в состав светильного газа; обычно очищенный светильный газ, получаемый пиролизом угля или нефти, содержит около 50% водорода, 34% метана, 8% окиси углерода, 4% непредельных углеводородов, 4% азота и 1% двуокиси углерода.
Громадные количества метана содержатся в некоторых месторождениях природных газов. В настоящее время успешна эксплуатируются такие месторождения близ Саратова, Ставрополя, Дашавы и др.; они снабжают газом, состоящим из почти чистого метана, Москву, Киев и другие большие города и промышленные центры, За последние годы на территории СССР открыт ряд новых месторождений природного метана.
Ввиду большой важности метана как вещества, лежащего в основе важнейшего ряда органических соединений, химики приложили много стараний, чтобы синтезировать метан из элементов. Впервые метан был получен из сероуглерода (легко получаемого синтетически из элементов) при пропускании его вместе с сероводородом через трубки с накаленной медью (Бертело, 1856):
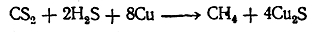
Лишь значительно позже (1897) было найдено, что метан может быть получен в качестве единственного продукта реакции непосредственным соединением углерода с водородом при 1200° С; в присутствии никеля эта реакция идет с хорошим выходом при более низкой температуре (475 °С).
Метан можно получить действием воды на карбид алюминия:
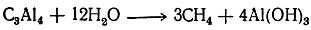
Это один из наиболее удобных способов получения метана в лаборатории. Он получается также восстановлением водородом окиси углерода или углекислого газа в присутствии металлического никеля при 250—400° С. Кроме того, метан можно получить по любому из общих способов получения углеводородов, и в лабораториях его часто получают сплавлением уксуснокислого натрия с едким натром.
Метан — бесцветный газ, без запаха, мало растворимый в воде, несколько лучше — в спирте. В 100 объемах воды при 20° С растворяется примерна 3,3 объема, а при 0° С — примерно 5,5 объема метана. Это — постоянный газ; его критическая температура —82,1°С при 45,8 ат. Горит он бледным синеватым пламенем.
При прохождении через раскаленные трубки, а также под действием искрового электрического разряда метан разлагается на водород и углерод, образуя, однако, при этом и некоторое количество более сложных углеводородов (этан, этилен, ацетилен, бензол, нафталин).
Пропусканием смеси метана с воздухом через нагретые трубки с различными катализаторами могут быть получены в качестве продуктов окисления метана метиловый спирт и муравьиный альдегид.
Хлор и бром на рассеянном свету замещают атомы водорода в метане, образуя, например, соединения СН3Сl, СН2Сl2, СНCl3 и СCl4. Под действием црямых солнечных лучей, а также при зажигании смеси метана с хлором происходит выделение углерода и образование хлористого водорода по уравнению
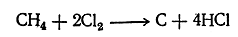
Некоторые физические свойства метана указаны выше (см. табл. 1).
Метан как главная составная часть природного газа является важным промышленным сырьем для получения ацетилена, хлорпроизводных (от хлористого метила до четыреххлористого углерода), формальдегида и нитро-метана.
Этан С2Н6
Этан С2Н6, так же как и метан, содержится в нефти и в газах, выделяющихся из земли в нефтеносных районах. Он содержится также в газах, получаемых сухой перегонкой каменного угля, и в газообразных продуктах крекинга и пиролиза нефти. В лабораториях этан обыкновенно получают восстановлением йодистого этила цинковой пылью в спиртовом растворе

или электролизом уксуснокислого натрия.
Этан — бесцветный газ, горящий слабо светящимся пламенем. Он может быть сгущен в жидкость уже при 4° С и давлении 46 ат. В воде он почти нерастворим; 1 объем абсолютного спирта растворяет 1,5 объема этана. При 575—650° С в отсутствие катализаторов этан разлагается на этилен и водород:
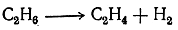
Пропан С3Н8
Пропан С3Н8 содержится во многих природных газах и частично образуется при крекинге нефти. Он применяется как газообразное и сжиженное горючее (особенно в смеси с бутаном), в качестве низкотемпературного растворителя и как сырье для нефтехимических синтезов. Широкое применение находят продукты пиролиза, окисления, хлорирования и нитрования пропана.
Бутан и изобутан С4Н10
Бутан и изобутан С4Н10 могут быть получены из тех же источников, что и пропан, и используются для тех же целей. Большие количества бутана подвергаются дегидрированию для получения бутадиена. Изобутан применяется также в реакциях алкилирования.


