Элиминирования реакции
ЭЛИМИНИРОВАНИЯ РЕАКЦИИ (р-ции отщепления), отщепление от молекулы орг. соед. частиц (атомов или атомных групп) без замены их другими. Различают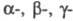 и d-элиминирования реакции. При
и d-элиминирования реакции. При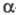 -элиминировании (отщепление частиц от одного атома) образуются валентно-ненасыщ. соед. (напр., карбены, нитрены), при
-элиминировании (отщепление частиц от одного атома) образуются валентно-ненасыщ. соед. (напр., карбены, нитрены), при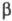 -элиминировании (отщепление частиц от соседних атомов) - соед. с кратными связями (С = С, С = С, С = N, C = N), при
-элиминировании (отщепление частиц от соседних атомов) - соед. с кратными связями (С = С, С = С, С = N, C = N), при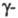 либо
либо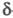 -элиминировании (отщепление частиц от атомов, разделенных одним или двумя атомами) - циклич. соед. Разновидность элиминирования реакций - выброс фрагмента из углеродной цепи или цикла с образованием новой
-элиминировании (отщепление частиц от атомов, разделенных одним или двумя атомами) - циклич. соед. Разновидность элиминирования реакций - выброс фрагмента из углеродной цепи или цикла с образованием новой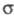 -связи (такие р-ции иногда наз. р-циями экструзии).
-связи (такие р-ции иногда наз. р-циями экструзии).
Наиб. изучены р-ции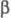 -элиминирования. Для них возможны 3 механизма - Е2, Е1 и Е1сВ (обозначение Е от англ. elimination). В р-циях бимол. элиминирования (механизм Е2) две группы отщепляются одновременно в одну стадию, при этом протон связывается с катализатором-основанием В:
-элиминирования. Для них возможны 3 механизма - Е2, Е1 и Е1сВ (обозначение Е от англ. elimination). В р-циях бимол. элиминирования (механизм Е2) две группы отщепляются одновременно в одну стадию, при этом протон связывается с катализатором-основанием В:
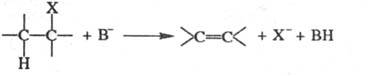
Р-ция стереоспецифична. Если группы Н и X находятся в антиперипланарном положении (см. Номенклатура стереохимическая), то при элиминировании они уходят в противоположном направлении; происходит т. наз. анти-элиминирование. Если же группы Н и X находятся в синперипланарном положении, то при элиминировании они уходят в одном направлении (син-элиминирование). анти-Элиминирование обычно предпочтительнее, чем син-элиминирование. Известно много примеров обоих видов элиминирования. Так, при элиминировании НВr из мезо-1,2-дибром-1,2-дифенилэтана образуется цис-2-бромстильбен, тогда как из рацемата получается транс-олефин. анти-Элиминирование эритро-соед. приводит к цис-олефинам, а трео-соед.- к транс-изомерам.
В нек-рых случаях, когда возможно образование ионных пар, а также под влиянием стерич., конформац. и других факторов происходит (а иногда даже преобладает) син-элиминирование. наиб. склонность к этим р-циям проявляют соед. с группой N(CH3)3.
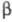 -Элиминирование галогеноводородов из алкилгалогенидов либо воды из спиртов подчиняются в основном Зайцева правилу (атом Н отщепляется от наименее гидрогенизир. атома углерода), а элиминирования реакции при термич. разложении четвертичных аммониевых оснований - правилу Гофмана (из неск. возможных олефинов образуется тот, к-рый содержит наименьшее число алкильных заместителей, обычно этилен; см. Гофмана реакции), напр.:
-Элиминирование галогеноводородов из алкилгалогенидов либо воды из спиртов подчиняются в основном Зайцева правилу (атом Н отщепляется от наименее гидрогенизир. атома углерода), а элиминирования реакции при термич. разложении четвертичных аммониевых оснований - правилу Гофмана (из неск. возможных олефинов образуется тот, к-рый содержит наименьшее число алкильных заместителей, обычно этилен; см. Гофмана реакции), напр.: 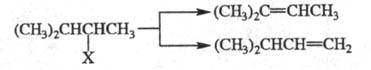
Мономол. механизм E1 - двухстадийный процесс, в к-ром медленная лимитирующая стадия - ионизация субстрата с образованием карбкатиона; последний быстро отдает протон основанию, к-рым часто служит р-ритель:
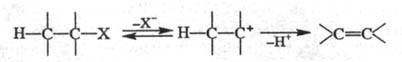
Обычно р-ции по механизму E1 идут без добавления основания, они нестереоспецифичны, т.к. прежде чем отдать протон, карбкатион может принять наиб. устойчивую конформацию.
По карбанионному механизму E1cB сначала отщепляется Н, а затем X. Это двухстадийный процесс, в к-ром интермедиатом служит карбанион:
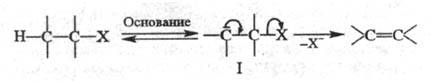
Обозначение механизма символом E1cB отражает участие в р-ции сопряженного основания ф-лы I (сВ - сопряженное основание, conjugated base). По механизму E1cB преим. реагируют субстраты, у к-рых водород активирован сильными электроноакцепторными группами.
Элиминирования реакции, протекающие в газовой фазе (пиролитич. элиминирование), могут происходить по перициклич. и свободнорадикальному механизмам.
О механизме фотохим. элиминирования реакций карбонильных соед. см. Фрагментации реакции.
Элиминирования реакции применяют в орг. синтезе для получения олефинов (см., напр., Бэмфорда-Стивенса реакция), а также циклич. соед., напр, образование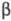 -лактамов из эфиров
-лактамов из эфиров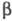 -аминокислот под действием реактива Гриньяра (р-ция Брекпота):
-аминокислот под действием реактива Гриньяра (р-ция Брекпота):
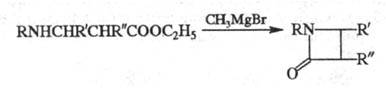
К элиминирования реакциям с образованием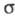 -связи относится, напр., превращение дибензилнитрозоамина в дибензил при действии дитионита натрия (р-ция Овербергера-Ломбардино):
-связи относится, напр., превращение дибензилнитрозоамина в дибензил при действии дитионита натрия (р-ция Овербергера-Ломбардино):
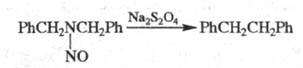
См. также Дегидратация, Дегидрогалогенирование, Хелетропные реакции.
Лит.: Общая органическая химия, пер. с англ., т. 1, М., 1981, с. 673-81; Mapч Дж., Органическая химия, пер. с англ., т. 4, М., 1988, с. 5-108.
