Нуклеиновые кислоты
НУКЛЕИНОВЫЕ КИСЛОТЫ (полинуклеотиды), биополимеры, осуществляющие хранение и передачу генетич. инфор-мации во всех живых организмах, а также участвующие в биосинтезе белков.
Первичная структура нуклеиновых кислот представляет собой последовательность остатков нуклеотидов. Последние в молекуле нуклеиновых кислот образуют неразветвленные цепи. В зависимости от природы углеводного остатка в нуклеотиде (D-дезоксирибозы или D-рибозы) нуклеиновые кислоты подразделяют соотв. на дезоксирибонуклеиновые (ДНК) и рибонуклеиновые (РНК) к-ты. В молекуле ДНК гетероциклы, входящие в остаток нуклеотида, представлены двумя пуриновыми основаниями - адeнином (А) и гуанином (G), и двумя пиримидиновыми основаниями - тимином (Т) и цитозином (С); РНК вместо Т содержит урацил (U). Кроме того, в нуклеиновых кислотах в небольших кол-вах обнаруживаются модифицированные (в осн. метилированные) остатки нуклеозидов- т. наз. минорные нуклеозиды, к-рыми особенно богаты транспортные рибонуклеиновые кислоты (тРНК). Отдельные нуклеотидные остатки связаны между собой в полинуклеотидных цепях 3'-5'-фосфодиэфирными связями (см. ф-лу). Стандартная запись нуклеотидной последовательности осуществляется в направлении от 5'-конца к 3'-концу (каждый нуклеотид обозначают буквой, присвоенной основанию, к-рое он содержит; напр., последовательность приведенного участка ДНК записывается как ACGT).
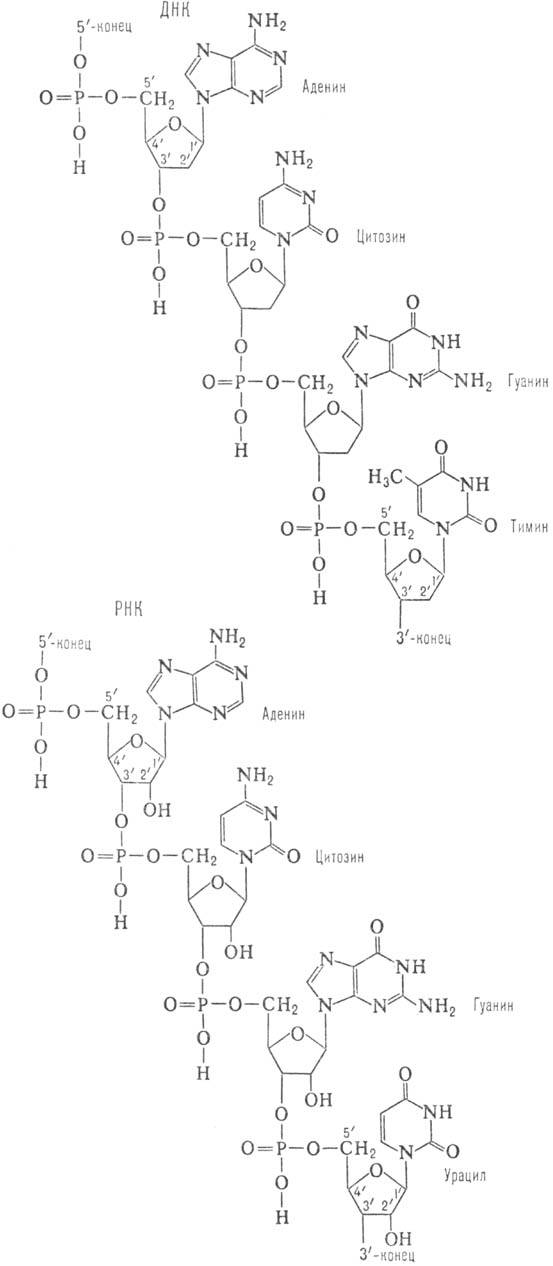
Св-ва ДНК и РНК различны. Так, РНК легко расщепляется щелочами до мононуклеотидов (благодаря наличию группы 2'-ОН), в то время как полинуклеотидные цепи ДНК в тех же условиях стабильны. Это структурное различие определяет и меньшую устойчивость к воздействию к-т N-гликозидных связей (связь между гетероциклом и остатком рибозы) в ДНК по сравнению с РНК.
Дсзоксирибонуклепновые кислоты. Нуклеотидный состав ДНК подчиняется ряду правил (т.наз. правила Чаргаффа), важнейшее среди которых - одинаковое содержание А и Т, G и С у любой клеточной ДНК. Нуклеотидный состав РНК подобным правилам не подчиняется.
Пространствю структура ДНК описывается как комплекс двух полинуклеотидных антипараллельных цепей (рис. 1), закрученных относительно общей оси, так что углевод-фосфатные цепи составляют периферию молекулы, а азотсодержащие гетероциклы направлены внутрь (д в о й н а я с п и р а л ь У о т с о н а-К р и к а). Антипараллельность полинуклеотидных цепей выражается в том, что на одном и том же конце спирали одна полинуклеотидиая цепь содержит (незамещенную или замещенную) группу 5'-ОН, а другая 3'-ОН. Фундам. св-во двойной спирали ДНК состоит в том, что ее цепи комплементарны друг другу (см. Комплементарностъ) вследствие того, что напротив А одной цепи всегда находится Т другой цепи, а напротив G всегда находится С. Комплементарное спаривание А с Т и G с С осуществляется посредством водородных связей. Классич. двойная спираль Уотсона-Крика получила назв. В-формы ДНК. Она-правозакрученная, плоскости гетероциклич. оснований перпендикулярны оси спирали, а число пар остатков нуклеотидов на один виток спирали равно примерно 10; расстояние между витками 3,4 нм. При изменении ионной силы и состава р-рителя двойная спираль изменяет свою форму и даже может превращ. в левозакрученную спираль (т.наз. Z-форму), к-рая содержит в одном витке ок. 12 остатков нуклеотидов. При дегидратации В-формы образуется А-форма ДНК-правозакрученная двойная спираль, содержащая в одном витке ок. 11 остатков нуклеотидов, плоскости гетероциклич. оснований повернуты примерно на 20° относительно перпендикуляра к оси спирали. Двойная спираль ДНК способна денатурировать (напр., при повышении т-ры) с полным расхождением комплементарных цепей, к-рые сохраняют способность к ассоциации с восстановлением (рекатурацией) двойной спирали при возвращении к исходным условиям. Подробно изучены также кон-формации фрагментов ДНК.
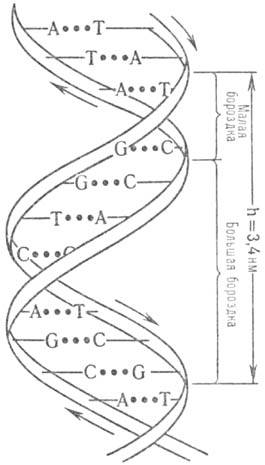
Рис. 1. Двойная спираль ДНК (стрелками показано направление полинуклеотидной цепи). .
Установлено, чго молекула ДНК в клетке представляет собой совокупность генов, регуляторных участков (последовательностей, связывающихся с регуляторными белками и управляющих уровнем экспрессии генов), районов, участвующих в организации генов в хромосомах, а также последовательностей, ф-ции к-рых еще не известны.
У прокариот (бактерии и синезеленые водоросли) ДНК организована в виде компактного образования-н у к л е о и-д а, к-рый содержит всю хромосомную ДНК клетки длиной в неск. миллионов пар нуклеотидов (м.п.н.). Кроме того, у мн. прокариот и эукариот (все организмы, за исключением прокариот) обнаружены нехромосомные ДНК (т. наз. плаз-миды)размером от неск. тысяч пар нуклеотидов (т.п.н.) до неск. десятков т.п.н. (м.п.н. и т.п.н.-принятые единицы длины двухцепочечной молекулы нуклеиновых кислот)-
Мн. ДНК образуют кольцевые структуры. В том случае, если обе полинуклеотидные цепи ДНК ковалентно непрерывны, ДНК может находиться в сверхспирализованной (сверхскрученной) форме (рис. 2). В клетках сверхспирализация осуществляется ферментами ДНК-гиразами (топоизомеразами II).
Хромосомные ДНК эукариот локализованы в клеточном ядре, где вместе с гистонами и негистоновыми белками образуют хроматин -ну-клеопротеид, из к-рого организованы хромосомы. Размеры ДНК в отдельных эукариотич. хромосомах колеблются в широких пределах-от 103 до 105 т.п.н.
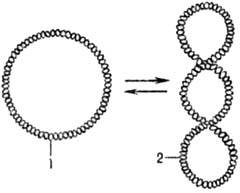
Рис. 2. Сверхспирализация двухцепочечной кольцевой ДНК под действием ДНК-гиразы: 1 - кольцевая форма ДНК; 2 - сверхспирализованная форма ДНК.
Геномы мн. вирусов бактерий (бактериофагов), животных и в более редких случаях растений представлены ДНК. Такие клеточные органеллы, как митохондрии и хлоропласты, имеют также свою собственную ДНК размером от неск. десятков до неск. сотен т.п.н.
Биосинтез ДНК осуществляется в результате репликации-точного самокопирования (самовоспроизведения) путем синтеза новой молекулы ДНК на исходной ("материнской"), к-рая играет роль матрицы. Этот процесс осуществляется под действием фермента ДНК-полимеразы. Матрицей для синтеза ДНК может служить также однотяжевая (одноцепочечная) РНК, комплементарное копирование к-рой осуществляет фермент обратная транскриптаза.
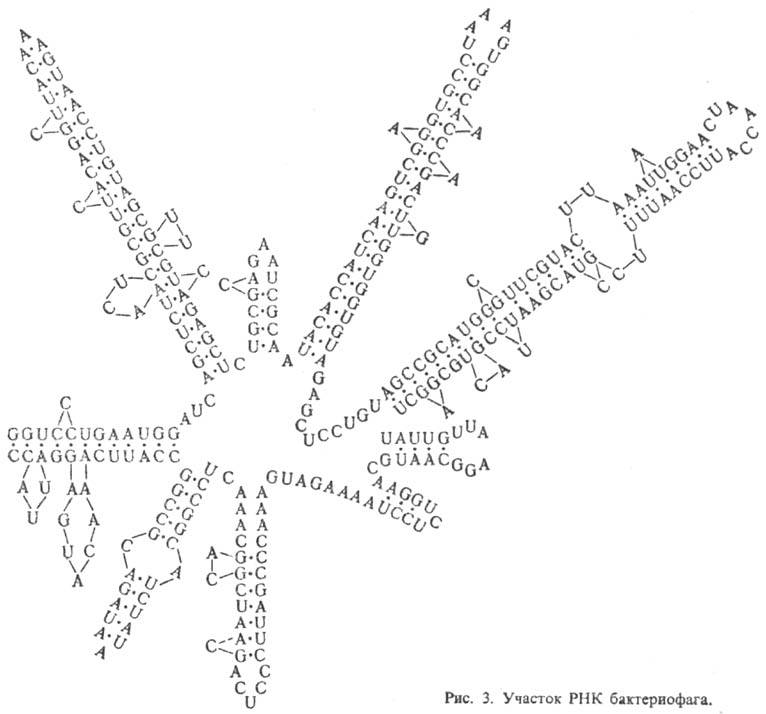
Рибонуклеиновые кислоты. РНК, как правило, построены из одной полинуклеотидной цепи, характерный элемент вторичной структуры к-рой - "шпильки", перемежающиеся однотяжевыми участками (рис. 3). Шпилька - двутяжевая спиральная структура, образующаяся в результате комплементарного спаривания оснований (А с U и G с С). Шпильки и соединяющие их одно-тяжевые участки РНК укладываются в компактную третичную структуру. Для тРНК вторичная структура имеет характерную форму, к-рую наз. "клеверным листом". Известны редкие примеры целиком двухспиральных молекул РНК.
Двухспиральные гибридные комплексы (ДНК и РНК) м.б. искусственно получены из комплементарных однотя-жевых ДНК и РНК. Функциональноактивные РНК имеют размер от 70-150 до неск. тысяч нуклеотидных остатков. Биосинтез РНК (транскрипция)обычно происходит в результате комплементарного копирования ДНК-матрицы, к-рое осуществляет фермент РНК-полимераза.
Известно неск. типов РНК. Рибосомные рибонуклеиновые кислоты, связываясь с рибосомными белками, образуют рибосомы, в к-рых осуществляется синтез белка. Матричные рибонуклеиновые кислоты служат матрицами для синтеза белков (трансляции). тРНК осуществляют связывание соответствующей аминокислоты и ее перенос к рибосомам. Обнаружены т.наз. малые ядерные РНК, участвующие в превращ. первичных продуктов транскрипции в функционирующие молекулы; т.наз. антисмысловые РНК участвуют в регуляции биосинтеза белка и репликации плазмидных ДНК. В виде РНК представлены геномы мн. вирусов (РНК-содержащие вирусы), в к-рых матрицами для синтеза РНК служат вирусные РНК. Нек-рые РНК обладают ферментативной активностью, катализируя расщепление и образование фосфодиэфирных связей в своих собственных или др. молекулах РНК.
Определение первичной структуры (секвенирование) нуклеиновых кислот. Секвенирование нуклеиновых кислот позволяет определить в одном эксперименте последовательность нуклеотидов в ДНК или РНК, содержащих неск. сотен мономерных звеньев. Методы основаны на общем принципе - определении с помощью высоко-разрешающего электрофореза в полиакриламидном геле с точностью до одного нуклеотида длины всех возможных фрагментов секвенируемого участка нуклеиновой кислоты, содержащих на одном конце одну и ту же последовательность нуклеотидов (гомогенный фрагмент), а на другом-один и тот же нуклео-тид. Такие фрагменты получают двумя разл. способами. В первом случае (метод Максама-Гилберта) гомогенный фрагмент ДНК или РНК, предварительно меченный радиоактивной меткой по одному из концов, расщепляют хим. агентами, специфичными к одному из четырех нуклеотидных остатков (A, G, С, Т или U); в случае РНК этот процесс осуществляют также специфич. рибонуклеазами. Расщепление ведут в таких ограничивающих условиях, когда в каждой молекуле нуклеиновой кислоты расщепляется только одна меж-нуклеотидная связь рядом с нуклеотидом данного типа, независимо от его положения в цепи. Такую операцию проводят для каждого из четырех нуклеотидных остатков и по длинам образующихся радиоактивных фрагментов определяют положение каждого нуклеотида в цепи нуклеиновой кислоты.
В др. случае (м е т о д С е н г е р а) используют олиго- или полинуклеотидную затравку (праймер) известной длины, коплементарную определенному участку нуклеиновой кислоты. Затравку наращивают с помощью ДНК-полимеразы, останавливая синтез на одном из четырех типов нуклеотидных остатков с равной вероятностью, независимо от его положения в цепи. Для этого к смеси четырех прир. субстратов ДНК-полимеразы добавляют т.наз. терминатор (обычно 2', 3'-ди-дезоксинуклеозидтрифосфат) - аналог определяемого нуклеотидного остатка, попадание к-рого на 3'-конец растущей цепи останавливает синтез. При этом радиоактивная метка вводится либо в затравку, либо в субстрат. Операцию повторяют для каждого из четырех нуклеотидов; длину образующихся радиоактивных фрагментов определяют стандартным способом. Эти методы в настоящее время удалось полностью автоматизировать (заменив в ряде случаев радиоактивную метку на флуоресцентную) и тем самым в тысячи раз повысить скорость секвенирования ДНК.
Получение нуклеиновых кислот. В клетках нуклеиновые кислоты связаны с белками, образуя нуклеопротеиды. Выделение нуклеиновых кислот сводится преим. к очистке их от белков. Для этого препараты, содержащие нуклеиновые кислоты, обрабатывают ПАВ и экстрагируют белки фенолом. Послед, очистка и фракционирование нуклеиновых кислот проводятся с помощью ультрацентрифугирования, разл. видов жидкостной хрома-тографии и гель-электрофореза. Для получения индивидуальных нуклеиновых кислот обычно используют разл. варианты последнего метода.
Совр. методы хим. синтеза нуклеиновых кислот позволяют получать крупные фрагменты ДНК, в т.ч. целые гены. Методич. основы хим.-ферментативных методов синтеза ДНК разработаны X. Кораной. Они включают: 1) хим. синтез комплементарных, взаимоперекрывающихся олигонуклеотидов, из к-рых затем в результате комплементационных взаимод. выстраиваются дуплексы - фрагменты молекулы синтезируемой ДНК с несовпадающими разрывами в обеих цепях; 2) соединение (лигирование) таких олигонуклеотидов в составе дуплекса с помощью фермента Т4 ДНК-лигазы. Сборку протяженных ДНК из синтетич. однотяжевых олигонуклеотидов проводят в неск. этапов (рис. 4). Сначала (а) собирают небольшие дуплексы с "липкими" концами (одно-тяжевыми комплементарными участками), из к-рых затем последовательно (б, в и т. д.) формируют более протяженные структуры. Т. обр. могут быть получены искусств. фрагменты ДНК большой длины и с любой нуклеотидной последовательностью. С помощью генетич. инженерии возможно клонирование (получение в индивидуальном виде и размножение) искусств. ДНК.
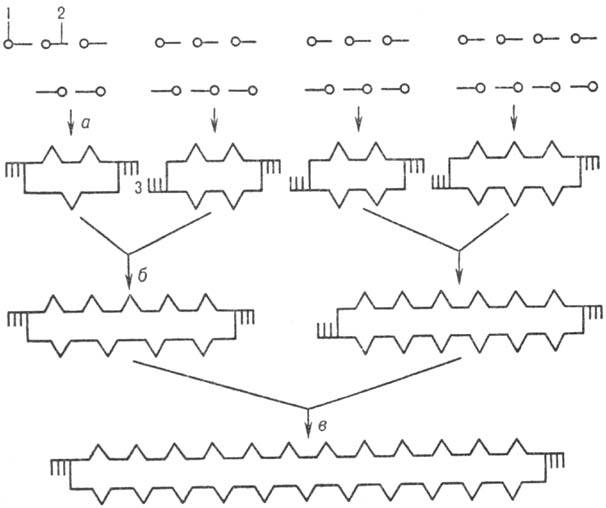
Рис.4. Схема синтеза полидезоксинуклеотида: 1,- соотв. 5'- и 3'-конец олигонуклеотидов; 3-комплементарные участки концов дуплексов (:липкие: концы); а,б и в-стадии образования дуплексов (все стадии катализируются Т4 ДНК-лигазой).
Синтез олигодезоксинуклеотидов Корана осуществил т. наз. фосфодиэфирным методом по схеме:
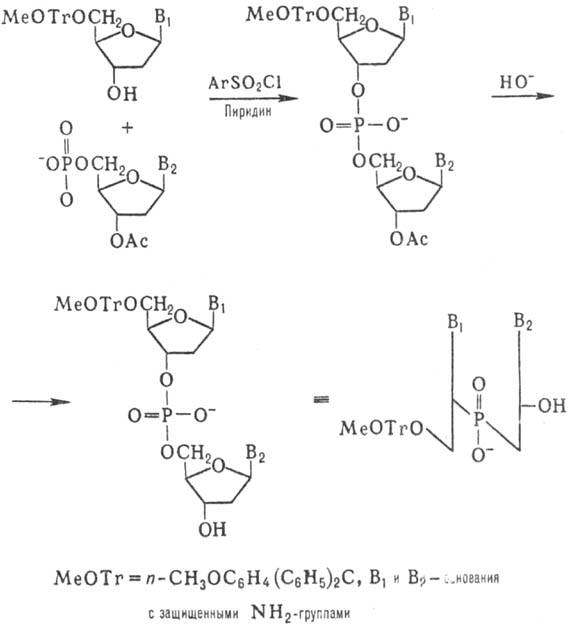
К динуклеотиду со своб. 3'-гидроксильной группой присоединяют таким же способом динуклеотид с незащищенной 5'-фосфатной группой и т.д. (т.наз. блочный метод синтеза):
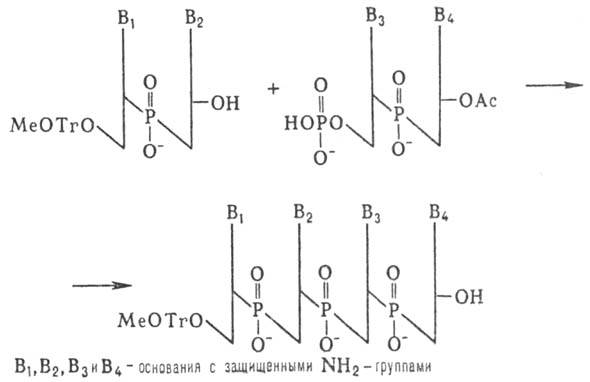
Несмотря на малую эффективность этого метода, были синтезированы олигонуклеотиды, содержащие до 16 звеньев, из к-рых были собраны первые синтетич. гены. Фосфоди-эфирный метод образования межнуклеотидных связей, использованный Кораной, имеет история, значение. Однако разработанные им приемы введения и избират. удаления защитных групп широко используются в др. методах синтеза нуклеиновых кислот.
Важным шагом в совершенствовании синтеза олигонуклеотидов явилась разработка т.наз. фосфотриэфирного метода, к-рый осуществляют по схеме:
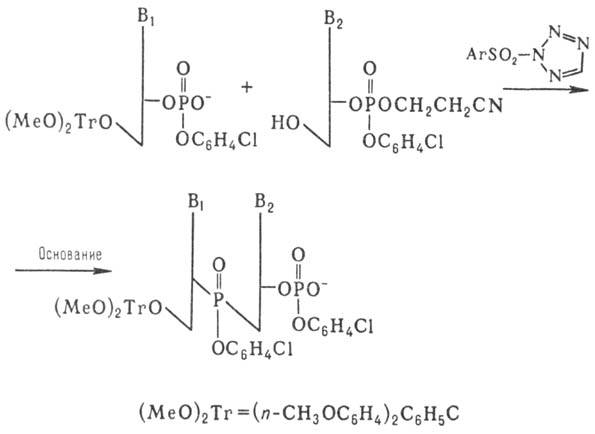
Образующийся динуклеотид далее (после частичного деблокирования фосфата) конденсируют аналогичным образом с др. динуклеотидом и т.д. Применение этого способа, в к-ром используют защиту фосфатной группы, позволило значит. сократить время синтеза и повысить выходы олиго-нуклеотидов.
Параллельно этим методам, к-рые осуществляют в р-рах, разрабатывались твердофазные способы синтеза нуклеиновых кислот. В последнем случае процесс проводят в двухфазной системе; нуклеозидный компонент связан ковалентно с нерастворимым полимером, а нуклеотидный компонент и необходимые реагенты находятся в р-ре.
Обычно в этом случае на первой стадии нуклеозид присоединяют с помощью "якорной" группы к нерастворимому полимеру. Затем его 5'-гидроксильную группу деблокируют и конденсируют с нуклеотидным компонентом. У образующегося полностью защищенного динуклеозидмонофосфата деблокируют защитную группу в положении 5' и присоединяют след. нуклеотид и т.д.
Наиб. распространенные методы твердофазного синтеза олигонуклеотидов основаны на использовании нуклеотидного компонента, содержащего Р(III). В т.наз. амидофосфитном-способе (рис. 5) нуклеотидным компонентом является эфир 3'-амидофосфита дезоксинуклеозида. Достаточно устойчивые амидофосфиты при протонировании в присут. тетразола превращ. в сильные фосфорилирующие агенты. Схема также включает блокирование непрореагировавшей 3'-гидроксигруппы достраивающегося олигонуклеотида (кэпирование) и окисление межнуклеотидного фосфита. На рис. показан один цикл наращивания цепи, к-рый длится 5-7 мин и далее повторяется. После завершения синтеза удаляют защитные группы с межнуклеотидных фосфатов, отделяют олигонуклеотид от носителя, деблокируют группы NH2 гетероциклов. Липофильную группу (МеО)2Тr удаляют после первого хроматографич. разделения.
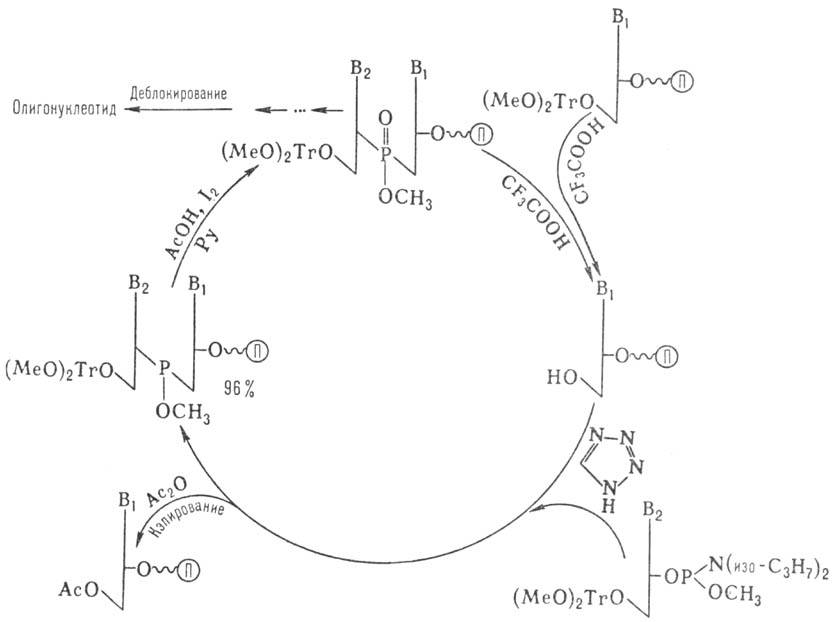
Рис. 5. Схема твердофазного синтеза олигонуклеотидов амидофосфитным методом; П - полимерный носитель, Ру- пиридин.
Др. метод основан на использовании гидрофосфориль-ного производного нуклеозида:
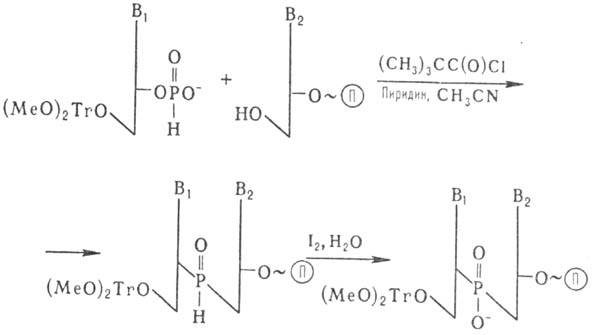
П-полимерный носитель
После снятия 5'-защитной диметокситритильной группы возможно присоединение след. нуклеотида. Окисление межнуклеотидных фосфитных групп проводят после завершения синтеза олигонуклеотида.
Стандартность операций в твердофазном синтезе олиго-нуклеотидов явилась основой для автоматизации процесса. Принцип работы автомата-синтезатора основан на подаче в реактор с помощью насоса (под контролем микропроцессора) защищенных нуклеотидных компонентов реагентов и р-рителей по заданной программе в колонку, содержащую полимерный носитель с закрепленным на нем первым нукле-озидом. После окончания синтеза и отделения полностью защищенного олигонуклеотида от полимерного носителя проводят деблокирование, очистку и анализ синтезир. фрагментов ДНК. Так, с помощью гидрофосфорильного метода
в автомате-синтезаторе за неск. часов получают 30-40-звен-ные олигонуклеотиды; возможен синтез более чем 100-звен-ных фрагментов ДНК. Разработаны синтезаторы, позволяющие проводить одновременно синтез неск. олигонуклеотидов.
Синтез олигорибонуклеотидов ферментативным путем осуществляют обычно с использованием рибонуклеаз (РНаз) или полинуклеотидфосфорилаз (ПНФаз). В первом случае р-цию осуществляют по схеме:
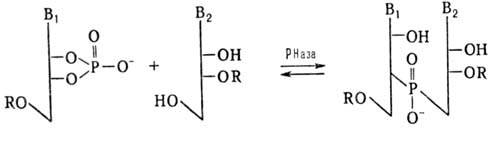
R-H или остаток олигорибонуклеотида
В качестве нуклеотидного и нуклеозидного компонентов применяют мономеры или олигонуклеотиды. Эту р-цию используют для синтеза ди-, три- и тетрарибонуклеотидов. При увеличении длины олигорибонуклеотида начинает преобладать обратная р-ция (гидролиз олигонуклеотида).
Для синтеза олигорибонуклеотидов с большим числом звеньев используют ПН Фазу:
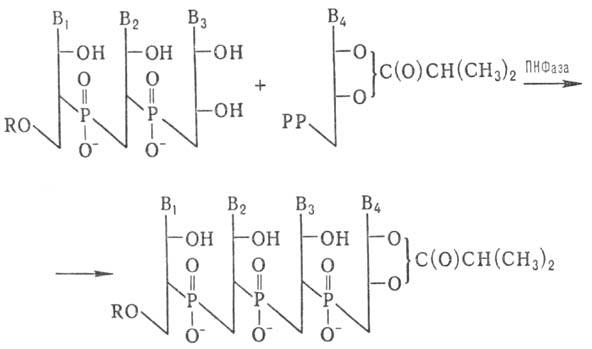
РР-Остаток пирофосфорной н-ты
Хим. синтез олигорибонуклеотидов проводят в осн. с использованием тех же приемов, как и при синтезе ДНК. Дополнит. трудности связаны с селективной защитой 2'-гидроксигруппы рибозы, а также с неустойчивостью фос-фодиэфирной связи РНК в щелочной среде.
Длинные фрагменты РНК получают из коротких, соединяя их с помощью РНК-лигазы.
Историческая справка. Нуклеиновые кислоты открыты в 1869-72 Ф. Мишером в ядрах (отсюда назв.: лат. nucleus-ядро) клеток гноя и в сперме лосося. В 1889 Р. Альтман выделил их в чистом виде (им же предложен термин "нуклеиновые кислоты"). В 1944 О. Эйвери показал, что с помощью ДНК наследств. признаки м. б. переданы от одной клетки к другой и что ДНК, т. обр., является "в-вом наследственности". Хим. строение нуклеиновых кислот изучалось школами А. Косселя, П. Левина, Дж. Гулленда и А. Тодда и было окончательно установлено к нач. 50-х гг. Макромол. структура ДНК (двойная спираль) установлена в 1953 Дж. Уотсоном и Ф. Криком на основании данных рентгеноструктурного анализа, полученных Р. Франклин и М. Уилкинсом. Нуклеотидный состав ДНК и РНК из многих объектов изучен Э. Чаргаффом и А. Н. Белозерским в 40-50-х гг. Изучение первичной структуры нуклеиновых кислот начато с сер. 60-х гг. с установления нуклеотидной последовательности тРНК (Р. Холли). Ф-ции большинства РНК установлены к нач. 60-х гг. Было показано, что они участвуют в реализации генетич. информации, закодированной в ДНК.
П. Доти и А. С. Спириным исследовано макромол. строение РНК. В сер. 70-х гг. разработаны эффективные методы расшифровки первичной структуры ДНК и РНК (методы Максама-Гилберта и Сенгера), к-рые в сочетании с методами генетич. инженерии позволили в течение след. десятилетия определить нуклеотидные последовательности мн. генов, плазмид, вирусных ДНК и РНК, рРНК и др. Разработаны приемы обработки этой информации с использованием ЭВМ. В 70-х гг. Кораной разработаны методы синтеза ДНК; им впервые синтезированы прир. гены (аланиновой и тиразиновой транспортных РНК). Начиная с сер. 70-х гг. создавались методы получения рекомбинантных нуклеиновых кислот (образуются, напр., в результате встраивания участка ДНК, в т.ч. гена, в плазмиду; см. Генетическая инженерия), к-рые существенно расширили возможности структурно-функцион. исследований нуклеиновых кислот и создали базу для использования достижений мол. биологии и генетики в биотехнологии. В 80-е гг. разработаны эффективные методы химического (в т.ч. автоматического) синтеза олигонуклеотидов и крупных фрагментов ДНК, к-рые широко используют для изучения структуры и ф-ций нуклеиновых кислот.
Лит.: Шабарова 3. А., Богданов А. А., Химия нуклеиновых кислот и их компонентов, М., 1978; Страйер Л., Биохимия, пер. с англ., т. 3, М., 1985; Уотсон Дж., Туз Дж., Курц Д., Рекомбинантные ДНК, пер. с англ., М., 1986; Зенгер В., Принципы структурной организации нуклеиновых кислот, пер. с англ., М., 1987; Овчинников Ю.А., Биоорганическая химия, М., 1987, с. 295-397. А. А. Богданов, 3. А. Шабарова.
