Установление строения полисахаридов
Что надо узнать?
Возвратимся к вопросу об установлении строения полисахаридов. Мы оставили рассмотрение его на стадии завершения мономерного анализа, включая результаты, полученные методом метилирования. Что же к этому моменту уже известно о структуре, а что еще предстоит узнать?
Известно, из каких моносахаридов построен полисахарид, в какой циклической форме их остатки входят в его состав, каково положение межмономерных связей в остатках каждого типа, каков тип структуры (разветвленный-неразветвленный). Для разветвленных полисахаридов, кроме того, известны степень разветвленности с структура точек ветвления. Это не мало, но это еще не структура. Что же еще не известно? Для всех типов полисахаридов – конфигурация гликозидных связей и последовательность расположения моносахаридных остатков в цепи, а также, за редкими исключениями, молекулярная масса. Для разветвленных полисахаридов к этому еще прибавляется вопрос о распределении остатков между основной и боковыми цепями, о длине боковых цепей и о положении различных точек ветвления (они могут располагаться в главной цепи, в первых от главной боковых цепях, во вторых от главной боковых цепях и т.д.). А для полисахаридов, имеющих неуглеводные заместители, надо еще установить положение этих заместителей. И только для одного – простейшего – типа полисахаридов мономерный анализ дает почти всю структурную информацию – для линейных регулярных полисахаридов, построенных из однотипно связанных остатков одного единственного моносахарида, каковы, например, целлюлоза и амилоза.
Совокупность нерешенных структурных вопросов можно несколько условно разбить на две группы: вопросы «ближнего» порядка в структуре и вопросы «дальнего порядка». Вот что мы имеем в виду. Выберем в полисахаридной цепи произвольным образом некоторый моносахаридный остаток А. Применяя те или иные методы, о которых речь впереди, можно узнать, с какими другими остатками он связан непосредственно: установить, например, наличие фрагмента …-Б-А-В-… как элемента структуры цепи. Сведения о ближнем порядке моносахаридных остатков в таком отрезке цепи, или, как говорят в полимерной химии, сегменте цепи, сами по себе мало что говорят о структуре всей макромолекулы. Однако знание структуры многих сегментов составляет уже обширную информацию о молекуле в целом. Обширную, но далеко не полную, потому что мы не знаем, как эти сегменты расположить в цепи относительно друг друга, и даже не можем сказать, существуют ли в цепи промежутки неизвестной структуры между известными нам сегментами. Этот вопрос можно отнести к дальнему порядку в структуре цепи, т.е. не о том, что находится на первом, втором и т.д. месте от данного остатка (ближний порядок), а о том, какие остатки располагаются от него в удалении, например, на двадцатом, тридцатом и т.д. месте. Схематически это можно пояснить так:
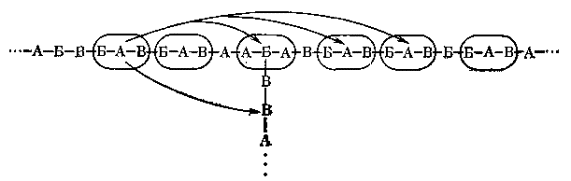
На схеме окружены примеры элементов ближнего порядка, стрелками указаны примеры элементов дальнего порядка.
Отвлекаясь пока от конкретных методов и приемов исследования, можно сказать, что для исчерпывающей характеристики структуры полисахаридной цепи нужно иметь полную информацию и о ближнем, и о дальнем порядке в макромолекуле. Существующие методы исследования нельзя четко разбить на две группы по характеру получаемого с их помощью ответа о ближнем или дальнем порядке (так сказать, на методы для ближнего порядка и методы для дальнего порядка). Тем не менее, мы постараемся оценить их информативность именно с этой точки зрения. А рассмотрев важнейшие структурные методы, обсудим сегодняшник возможности установления структуры полисахаридов в целом.
Как узнать?
Общий принцип выяснения последовательности моносахаридных остатков в полисахариде состоит в расщеплении цепи на олигосахаридные фрагменты, установлении строения таких фрагментов и последующей реконструкции структуры макромолекулы по структурам олигосахаридов. Вот два характерных примера применения этого принципа, на которых можно проследить его возможности и ограничения.
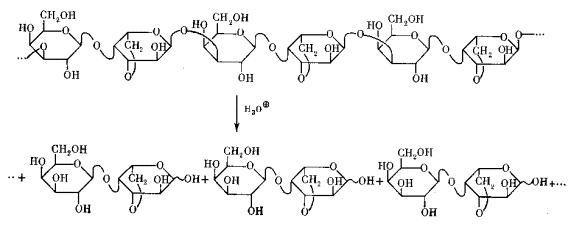
В агарозе имеются гликозильные остатки двух видов: β -D-галактопиранозильный и 3,6-ангидро- α -L-галактопиранозильный. Гликозидная связь второго из них гораздо более чувствительна к кислотному гидролизу и некоторым другим аналогичным реакциям расщепления. Поэтому в определенных условиях можно добиться ее избирательного разрыва, не затрагивая при этом гликозидную связь остатка β -D-галактопиранозы. В результате полисахаридная цепь распадается на дисахаридные блоки агаробиозы по схеме, приведенной на.
Образование именно такого дисахарида с полной определенностью указывает на присутствие в исходной цепи отвечающей ему последовательности β -D-галакторираноза-3,6-ангидро-L-галактопираноза, а высокий выход этого дисахарида означает, что такая последовательность доминирует в цепях. Поскольку из мономерного анализа мы знаем, что два вида моносахаридных остатков входят в состав агарозы в соотношении 1:1, доминирование такого сегмента возможно только в структуре цепи с чередующимися остатками. Таким образом, мы узнаем о наличии второго типа сегмента: 3,6-ангидро-L-галактопираноза-
β -D-галактопираноза. Схематически это можно представить так:

где Г-остаток β -D-галактопиранозы, А-остаток 3,6-ангидро- α -L-галактопиранозы.
В результате анализа полисахарида при помощи такого частичного гидролиза мы получаем, как видно, надежную информацию о ближнем порядке моносахаридных остатков в цепи, т.е. о том, какой остаток с каким связан непосредственно. Мы однако, остаемся в неведении относительно дальнего порядка, что применительно к нашему примеру сводится к вопросу о регулярности строения цепи. Почему же мы не вправе решить его утвердительно на основании приведенных выше данных? Сейчас разберемся.
Если бы избирательность разрыва гликозидных связей при частичном гидролизе была абсолютной, а выход дисахарида – количественным, то из таких результатов можно было бы сделать вполне строгий вывод о регулярности структуры агарозы. Однако даже тогда, когда мы имеем дело с агарозой (случай, совершенно исключительный для всей химии углеводов по степени избирательности химического гидролиза), выход агаробиозы не достигает 100%. Следовательно, мы вправе предполагать наличие в цепи каких-то других последовательностей, помимо тех существование которых мы установили экспериментально. Например, с результатами эксперимена вполне совместимо предположение о наличии некоторого количества сегментов …-А-А-… и …-Г-Г-…, которые по тем или иным причинам не обнаруживают себя при частичном гидролизе:
…-А-Г-А-Г-А-Г-А-А-Г-А-Г-А-Г-А-Г-Г-
-А-Г-А-Г-А-Г-А-Г-…
Правомерность такого предположения не позволяет нам утверждать, что на основании описанного эксперимента мы установили дальний порядок связей. Мы можем лишь говорить о том, что правильное чередование остатков доминирует в структуре полисахарида.
Значительное различие в скоростях кислотного гидролиза входящих в полисахарид гликозидных связей – явление сравнительно редкое. Во всяком случае, та степень избирательности, которая достигается для агарозы, уникальна. В типичных же случаях выходы олигосахаридов при частичном гидролизе гораздо ниже и, следовательно, по информативности результатов такие эксперименты значительно уступают рассмотренному примеру.
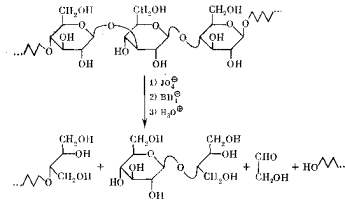
Другой метод частичного расщепления полисахаридных цепей (деградация по Смиту) основан на более избирательной, но и более сложной последовательности реакций. Ключевой стадией здесь служит окисление полисахарида солями иодной кислоты – периодатами. При этой реакции происходит разрыв С-С-связи в гликолях с образованием диальдегида, последующее восстановление которого приводит к образованию диола, как показано на схеме:
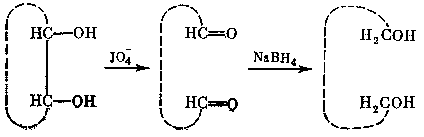
Строго обязательным условием для периодатного окисления является наличие двух гидроксильных групп у соседних углеродных атомов, между которыми и разрывается С-С-связь. Моносахаридное звено в цепи, содержащее систему такого гликоля, расщепляется до ациклического ацеталя, как показано на примере β -D-глюкопиранозильного звена с заместителем (например, левой частью полисахаридной цепи) в положении 4.
Ациклический ацеталь, образующийся при этих реакциях из окисленного моносахаридного звена, сравнительно легко подвергается кислотному гидролизу, так что последний удается провести высоко избирательно, т.е. не затрагивая
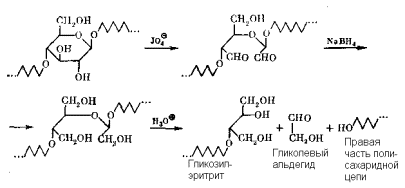
обычные гликозидные связи. В результате происходит разрыв полисахаридной цепи по окисленному звену. При этом левая часть цепи превращается в гликозид многоатомного спирта (в нашем случае эритрита), а в правой появляется концевое моносахаридное звено, которое раньше не было связано с окисленным остатком.
Теперь рассмотрим деградацию по Смиту неразветвленного глюкана из овса, в состав которого входит два типа остатков β -D-глюкопиранозы со связями 1 à 3 и 1 à 4. Первое из этих звеньев устойчиво к действию периодата, так как не содержит подходящих гликольных группировок, а окисление второго мы только что обсуждали.
Оценим сначала, каких результатов периодатного окисления для основных типов структуры полисаханида, которые можно умозрительно построить на основании данных мономерного анализа. При правльном чередовании 1 à 3- и 1 à 4-связанных остатков главными продуктами деградации должны быть глюкозил-эритрит и гликолевый альдегид, образующиеся в результате сохранения 1 à 3-связанного звена и окисления двух примыкающих к нему остатков со связями 1 à 4 .
При блочном строении цепи, т.е. наличии в ней длинных последовательностей из 1 à 3- и 1 à 4-связанных остатков, первые должны приводить к образованию полимерного неокисленного фрагмента, а вторые – полностью распадаться до свободного эритрита и гликолевого альдегида. Наконец, при хаотическом распределении остатков продуктом деградации должна быть смесь низкомолекулярных гликозил-эритритов, образующихся из коротких последовательностей 1 à 3-связанных остатков, гликолевого альдегида, а также свободного эритрита, возникающего
при окислении коротких последовательностей остатков со связями 1 à 4. Эксперимент показывает что реализуется именно этот третий случай. Действительно, глюкан овса при деградации по Смиту распадается на серию мономерных и олигомерных фрагментов, анализ которых позволяет вывести ряд заключений о его структуре (см. схему)
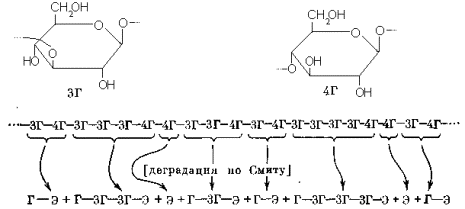
3Г,4Г – остатки глюкопиранозы, замещенные в положении 3 и 4 соответственно; Г – концевое (незамещенное) глюкопиранозное звено; Э – остаток эритрита или свободный эритрит.
Из того факта, что все содержащие глюкозу фрагменты имеют на восстанавливающем конце остаток эритрита (а не какого-нибудь другого полиола) следует, что в полисахариде существует связь 3Г-4Г. Наличие таких фрагментов, содержащих два, три и четыре остатка глюкозы, указывает на присутствие в цепи последовательностей из двух, трех и четырех остатков типа 3Г, расположенные подряд. С другой стороны, то, что все продукты деградации низкомолекулярны, свидетельствует об отсутствии в полисахариде длинных последовательностей из таких неокисляемых остатков. Образование свободного эритрита указывает на существование сегментов …-4Г-4Г-…, однако в отличие от последовательностей …-3Г-3Г-… не позволяет сделать никаких заключений об их длине. Определение выходов полученных фрагментов всех типов дает возможность оценить относительное содержание соответствующих сегментов в исходном полисахариде, а их разнообразие указывает на отсутствие простой регулярности в чередовании различных остатков в цепи.
Таким образом, деградация по Смиту позволяет узнать очень многое о ближнем порядке в структуре полисахарида, включая последовательности из нескольких моносахаридных звеньев. Однако о дальнем порядке мы можем сказать еще меньше, чем в случае частичного гидролиза агарозы. Действительно, найденные сегменты цепей могут быть сгруппированы в блоки, могут чередоваться по определенному (достаточно сложному) закону, могут, наконец, распределяться по цепи хаотически. Обо всех этих характеристиках дальнего порядка мы остаемся в неведении.
Два разобранных примера частичного расщепления полисахаридных цепей по информативности характерных для всего цикла методов фрагментации такого типа. С их помощью можно узнать многое или почти все о ближнем порядке в структуре и кое-что или почти ничего о дальнем порядке. Тем не менее, применение к одному полисахариду разных методов фрагментации, в особенности таких, которые обеспечивают расщепление разных связей, весьма существенно обогащает информацию, получаемую каждым из этих методов порознь. Например, если из последовательности …-А-А-Б-В-Г-Д-А-А-Д-Г-Г-Б-… одним методом были получены фрагменты А-А-Б-В-Г, В-Г-Д, Д-Г-Г-Б, а другим – фрагмент Г-Д-А-А-Д-Г, то в совокупности эти данные определяют всю додекасахаридную последовательность, т.е. дают сведения о точной структуре уже довольно значительного сегмента цепи.
Мы еще ничего не сказали о способах определения конфигурации гликозидных связей моносахаридных остатков в полисахаридных цепях. Между тем этот вопрос нередко оказывается камнем преткновения во всем структурном анализе полисахаридов.
Выяснение конфигурации гликозидных связей – это по существу задача мономерного анализа, так как относится не к характеристике структуры цепей, а к детализации структуры отдельных звеньев. Тем не менее известными сейчас методами мономерного анализа эта задача не решается. Дело в том, что все эти методы по своей сути деструктивны и обязательно включают расщепление гликозидных связей. А при всех известных способах расщепления гликозидных связей, применяемых в мономерном анализе полисахаридов (кроме ферментативного гидролиза, см. ниже), информация о конфигурации этой связи теряется.
Мы уже упоминали, что гликозидный центр вносит наибольший вклад в величину удельного вращения углеводов. Поэтому из величины удельного вращения полисахарида можно сделать некоторые заключения о конфигурации гликозидных связей входящих в него моносахаридных остатков. Однако, поскольку удельное вращение – величина аддитивная, такие заключения неизбежно носят усредненный характери, т.е. ничего не говорят о том, какие именно остатки имеют α - или β -конфигурацию. Лишь в простых и крайних случаях оптическая активность полисахарида позволяет сделать более определенные выводы. Действительно, по величине удельного вращения можно достаточно уверенно сделать заключение о преобладании гликозидных связей с такой-то конфигурацией в полисахаридах, построенных из однотипных моносахаридных остатков с одной конфигурацией гликозидных связей.
Совсем по-другому выглядит задача определения конфигурации гликозидных связей в олигосахаридах, особенно в низших олигосахаридах, получаемых при тех или иных способах фрагментации полисахаридных цепей. Дело в том, что при малом количестве гликозидных связей (в дисахаридах, например, такая связь только одна) удельное вращение уже позволяет с гораздо большей определенностью судить о конфигурации этих связей. Кроме того, в ди-, три-, а при удаче и в тетрасахаридах можно определить конфигурацию гликозидных центров с помощью спектроскопии ПМР, подобно тому, как это делается в низших гликозидах.
По-видимому, универсальный (гипотетический) метод определения конфигурации гликозидных связей в полисахаридах можно представить себе следующим образом. Это должен быть такой метод расщепления гликозидных связей, который приводил бы количественно к производным моносахаридов, подобно кислотному гидролизу. Но с той, однако, разницей, что структура этих производных должна зависеть от конфигурации расщепляемой гликозидной связи исходного остатка. Тогда мы имели бы метод мономерного анализа, который одновременно давал бы информацию и о природе каждого мономерного звена, и о конфигурации его гликозидной связи. К сожалению, ничем похожим на такое идеальное решение углеводная химия пока не располагает (хотя препятствий принципиального характера к разработке подобного метода не видно). Наилучшее доступное сейчас приближение к идеалу – это окисление ацетатов полисахаридов хромовым ангидридов в уксусной кислоте. Суть этого метода состоит в следующем.
Глюкопиранозильный остаток, гидроксилы которого защищены от окисления ацетилированием, при обработке хромовым ангидридом в уксусной кислоте претерпевает окисление, при котором гликозидная связь превращается в сложноэфирную. Остаток моносахарида превращается при этом в остаток кетоальдоновой кислоты. В эту реакцию вступают только гликозильные остатки, у которых водород при гликозидном центре аксиален (см. схему на с. 97). Поэтому из двух возможных аномеров моносахаридного остатка внутри полисахаридной цепи окислению подвергается только один. Если далее такой окисленный полисахарид подвергнуть мономерному анализу, то по исчезновению тех или иных моносахаридов из гидролизата (по сравнению с исходным полисахаридом) можно судить о том, что именно эти остатки в полисахаридной цепи имели «окисляемую» конфигурацию (с аксиальным водородом при С-1), а сохранившиеся – «неокисляемую» (с экваториальным водородом при С-1).
Описанный метод установления конфигурации гликозидных связей достаточно эффективен и широко применяется сейчас в структурных исследованиях за неимением лучшего. В нем, однако, заложено принципиальное несовершенство
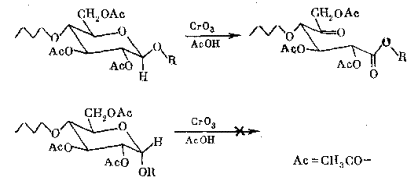
Дело в том, что конформация моносахаридного звена в ацетилированной полисахаридной цепи обычно закреплена не жестко, так что даже при значительной предпочтительности одной конформации данного звена (например, с экваториальным водородом при С-1) оно в растворе может принимать, по крайней мере кратковременно, и противоположную конформацию (с аксиальным водородом при С-1). При этом «неокисляемое» звено, не меняя конфигурацию гликозидной связи, превращается в «оксиляемое» (см. схему). За счет этого строгая избирательность
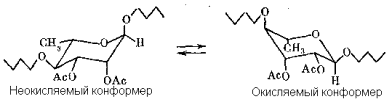
реакции нарушается, и результаты такого анализа приходится трактовать не в четких терминах «да»-«нет», а в более осторожных: «преобладает»-«имеется в небольшом количестве». Более того, в определенных случаях анализ полисахаридов этим методом приводит и к прямо ошибочным заключениям: по видимому, вследствие значительных конформационных искажений звеньев за счет влияния всей полисахаридной цепи в целом.
Рассмотрим еще один путь исследования структуры полисахаридов, претераевающий в настоящее время бурное развитие и представляющийся исключительно перспективным: спектроскопию ЯМР на ядрах 13 С. Природный углерод состоит из трех изотопов: 12 С, 13 С и 14 С. Главный компонент 12 С и радиоактивный изотоп 14 С не дают сигнала в спектрах ЯМР, однако ядра 13 С, имеющие полуцелый спин, дают такой сигнал. Содержание изотопа в природном углероде мало (1,1%). С одной стороны, это обстоятельство технически существенно осложняет спектроскопию на этих ядрах, а с другой – приводит к резкому упрощению картины спектров по сравнению со спектрами резонанса на протонах.
Дело в том, что в обычных органических молекулах ядра 12 С и 13 С располагаются во всех возможных положениях по закону случая. Поэтому появление двух ядер 13 С в соседних положениях молекулы – событие маловероятное (вероятностью 0,0121%). В результате спин-спиновые взаимодействия 13 С- 13 С практически не оказывают влияния на картину спектров ЯМР 13 С, т.е. каждое такое ядро дает в спектре синглет (спин-спиновые взаимодействия с соседними протонами подавлены благодаря спекиальной технике съемки спектров).
Кроме того, величины химических сдвигов ядер 13 С и различия между этими величинами велики по сравнению с величинами химических сдвигов протонов. Поэтому ЯМР-спектр на ядрах 13 С представляет собой набор достаточно хорошо разрешенных синглетов, что резко облегчает интерпретацию спектра. Величина химического сдвига определяется, как обычно, всем окружением данного ядра. В моносахаридах нет эквивалентных (в смысле химического окружения) положений углеродных атомов. В результате, например, 13 С ЯМР-спектр глюкозы состоит из шести хорошо разрешенных синглетов, отвечающих шести атомам углерода. Более того, спект равновесной смеси α- и β -D-глюкопираноз (уравновешенная по мутаротации D-глюкоза) представляет собой результат наложения двух независимых спектров аномеров, т.е. состоит из 12 сигналов.
При этом особенно важно, что присоединение гликозильного остатка к одному из атомов кислорода приводит к резкому (до 10 м.д.) изменению химического сдвига соответствующего ядра 13 С, что позволяет определять положение межмономерных связей в полисахаридных цепях. Понятно, что основанный на такой спектроскопии метод обладает колоссальными возможностями для изучения полисахаридных структур. Разберем в качестве примера спектр агароподобного полисахарида одной из красных водорослей.
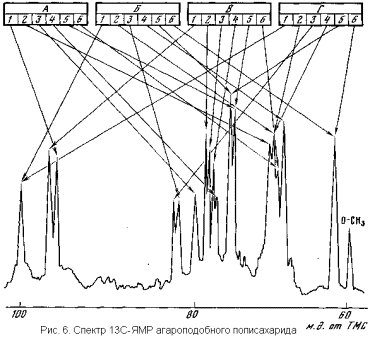
Участок цепи, отражающий основные особенности структуры этого полисахарида, представлен на схеме, а его спектр – на рис.6.
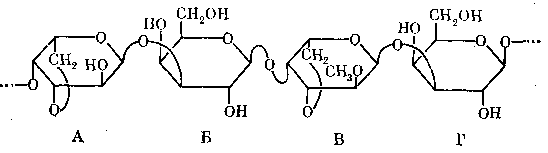
В состав полисахарида входит четыре типа моносахаридных остатков (А-Г), различающихся по структуре или по окружению в цепи. Эти остатки содержат 25 химически различимых атомов углерода, в спектре же имеется 18 четко разрешенных сигналов. Таким образом, большинство углеродных атомов дает индивидуальные сигналы, хотя меньшая часть из них – сигналы с перекрывающимися химическими сдвигами. Анализ спектра показывает (отнесения сигналов представлены на рисунке), что каждому из четырех моносахаридных звеньев соответствует, по крайней мере, один сигнал, свойственный углеродным атомам этого остатка, а углеродные ядра остатка А дают даже четыре сигнала, не перекрывающиеся ни с одним из сигналов других остатков и, следовательно, характерные только для него. Такой хорошо разрешенный спектр позволяет непосредственно установить природу моносахаридных остатков входящих в состав подобного полисахарида, положение межмономерных связей и конфигурацию гликозидных связей. Более того, по спектру можно измерить относительное содержание различных типов остатков в цепи.
Еще более интересно то, что химический сдвиг определенных ядер 13 С в моносахаридных остатках зависит не только от структуры самого остатка, но и от структуры других звеньев, связанных с ним гликозидной связью. Так, остатки Б и Г (см. с. 99), взятые изолированно, представляются химически эквивалентными. Однако первый из них гликозилирован в положении 3 остатков 3,6-ангидро-L-галактозы (А), а второй – остатков 2-О-метил-3,6-ангидро-L-галактозы (В). В связи с этим химические сдвиги ядер С-3 остатков Б и Г оказываются различными (82,2 и 82,7 м.д. соответственно). Такая чувствительность положения сигналов в спектре 13 С ЯМР к окружению моносахаридного звена открывает захватывающие возможности для определения последовательности остатков в цепи.
Таким образом, спектроскопия ЯМР на ядрах 13 С позволяет не только определять природу, тип связи, конфигурацию гликозидных остатков, входящих в состав биополимера, т.е. решать задачу мономерного анализа, но и устанавливать ближний порядок в расположении этих остатков в цепи, т.е. получать информацию, извлекаемую обычно из методов фрагментации. Принципиально важно, что такой анализ является неразрушающим. Поэтому весь полисахарид, использованный для съемки спектра, возвращается к исследователю в неизменном виде. В свете сказанного можно полагать, что в ближайшем будущем этот метод исследования станет одним из ведущих для изучения полисахаридных структур и заставит классические деструктивные методы значительно уступить свои позиции.
Мы рассмотрели несколько методов структурного анализа полисахаридов. Они далеко не исчерпывают всего арсенала инструментов исследования в этой области, но характеризуют многие важные принципы такого исследования. В смысле возможностей выяснения ближнего порядка моносахаридных звеньев в цепях и их дальнего порядка, а также оценки общего плана построения макромолекулы эти методы информативны далеко не в равной степени. Если, как мы видела, для характеристики ближнего порядка эти методы вполне пригодны, то с вопросами дальнего порядка дело обстоит гораздо менее благополучно. В сущности, все эти методы (заметим еще раз, основные методы структурного анализа полисахаридов) позволяют узнать о дальнем порядке очень мало, по крайней мере в общем случае. Это, однако, не эквивалентно бессилию современной науки перед проблемой установления структуры сложных полисахаридов. Есть несколько эффективных подходов к определению общей схемы построения цепей и дальнего порядка звеньев, хотя и носящих более частный характер, чем разобранные выше методы. Вот один из примеров.
В разветвленных полисахаридах довольно частый случай – расположение более лабильных к кислотному гидролизу звеньев в боковых цепях и более прочных – в главной цепи. Тогда при частичном гидролизе можно получить набор моносахаридов и низших олигосахаридов из боковых цепей и полимерный материал главной цепи. Такой результат позволяет сразу установить, каково в общих чертах распределение определенных типов остатков между главной и боковыми цепями, а также, что не менее важно, получить достаточные количества полисахарида упрощенной структуры (такие полимерные фрагменты часто называют деградированными полисахаридами) и установить его строение, т.е. решить уже более простую задачу, чем установление строения нативного (неизмененного) полисахарида.
Итак, мы видим уже два принципа установления структуры сложных полисахаридов: с одной стороны, путь от мономерного анализа, через расщепление на олигосахаридные блоки и реконструкцию последовательности моносахаридных остатков во все более длинных сегментах цепей, а с другой – путь от общего представления о макромолекуле, как о целом, через последовательную локализацию целых групп или типов моносахаридных остатков в определенных крупных элементах структуры (в главной цепи, в боковых цепях, в узлах и т.д.) и до локализации отдельных моносахаридов в определенных положениях этих цепей. Есть еще и третий путь, в некоторых случаях дающий весьма обширную информацию о структуре. Он связан с применением ферментов, которые катализируют расщепление полисахаридных цепей.
Главная особенность ферментов, как инструментов структурного анализа полисахаридов – высокая, в некоторых случаях абсолютная, спекифичность их действия. Ферменты, расщепляющие полисахариды (полисахаридазы), как правило абсолютно специфичны к конфигурации гликозидной связи (например, фермент настроенный на гидролиз α -гликозидной связи, совершенно не действует на β -гликозидные связи), абсолютно специфичны к размеру цикла моносахаридного остатка и высоко спекифичных к структуре и конфигурации самого моносахаридного звена. Кроме того, и это особенно важно для установления строения полисахаридов, полисахаридазы обычно высоко избирательны к типу связей и к структуре остатков в ближайшем окружении к расщепляемой гликозидной связи. Поэтому уже сам факт расщепления определенной связи данным ферментов нередко дает много сведений о ближнем порядке остатков в этом участке цепи (пример такой избирательности лизоцима мы уже рассматривали в другом аспекте).
Ферменты, расщепляющие полисахариды, бывают двух типов – эндоферменты и экзоферменты. Первые катализируют гидролиз некоторых гликозидных связей внутри полисахаридной цепи, т.е. расположенные достаточно далеко от обоих ее концов. Вторые способны вызывать гидролитическое отщепление только концевых моносахаридных остатков (в некоторых случаях концевых дисахаридных фрагментов). Не нужно думать, что процесс на этом останавливается: в полученном укороченном полисахариде есть свое концевое звено, которое в свою очередь подвергается атаке ферментом, если обладает нужной структурой и конфигурацией.
Как же можно использовать полисахариды в структурных исследованиях? Эндоферменты – это прежде всего реагенты для высоко избирательной фрагментации полисахаридных цепей; причем в отличие от кислотного гидролиза такое избирательное расщепление позволяет делать заключение и о конфигурации разорванной гликозидной связи, и о природе самого гликозильного остатка, и нередко о его ближайшем окружении в цепи. Таким образом, это весьма эффективный метод и получения фрагментов, и определения ближнего порядка моносахаридных звеньев. Гидролиз разветвленных полисахаридов экзоферментами может служить тонким и специфичным методом получения деградированных полисахаридов путем избирательного отщепления боковых цепей. Для расщепления цепей, особенно в неразветвленных полисахаридах, экзоферменты иногда открывают уникальные возможности установления регулярности, т.е. дальнего порядка звеньев. Насколько мощным является данный инструмент, можно судить по следующему примеру.
Экзофермент, катализирующий гидролиз β -D-глюканов с 1 à 3-связями, в частности ламинарина, до глюкозы (избегая строгой номенклатуры, назовем его ламинаразой), высоко специфичен к типу гликозидных связей, т.е. расщепляет только связи 1 à 3. Поэтому, если изучаемый полисахарид под действием лиминаразы претерпевает полный гидролиз, можно уверенно утверждать, что он имеет регулярную структуру и построен только из β -D-глюкопиранозных звеньев, соединенных 1 à 3-связями. Иными словами, исследование полисахарида при помощи ферментативного гидролиза дает сразу сведения и о мономерном составе, включая конфигурацию и положение межмономерных связей, и о ближнем порядке звеньев, и о дальнем порядке остатков в цепях. На первый взгляд может показаться, что применительно к регулярному неразветвленному полисахариду ферментативный гидролиз дает информацию такого же характера, что и обычный мономерный анализ при помощи метилирования (если отвлечься от конфигурации гликозидных связей). Мы сейчас увидим, однако, что это не соответствует действительности.
Допустим, мы изучаем глюкан со степенью полимеризации (числом моносахаридных остатков в цепи) 100. В результате его анализа методом метилирования в нем были обнаружены только 1 à 3-связи и не обнаружено других. Однако «не обнаружено» – понятие довольно неопределенное. Его истинный смысл можно оценить, только зная чувствительность примененных аналитических методов. В нашем случае это чувствительность обнаружения минорных компонентов в смеси производных метилированных моносахаридов. Для существующих сейчас методов анализа таких смесей оценка нижнего предела чувствительности в 1% очень хорошая. Это значит, что мы вполне могли не заметить одного «аномального» звена (например, 1 à 4-связи) на каждую полисахаридную молекулу. Таким образом, вывод о строгой регулярности строения на основании таких данных будет весьма шатким. Теперь посмотрим, что даст для такого полисахарида ферментативный гидролиз.
Экзоламинараза гидролизует такой полисахарид, последовательно отщепляя от него по одной молекуле глюкозы, начиная с невосстанавливающего конца. Если в цепи встретится одно «аномальное» звено (например, звено с 1 à 4-связью), то ферментативный гидролиз в этом месте прекратится и (это очень важно заметить) вся остальная часть полисахаридной молекулы останется нерасщепленной. Действительно, у такого «огрызка» цепи концевое звено аномальное и фермент перестает на него действовать, как показано на схеме этапов последовательного гидролиза полисахарида экзоферментом.
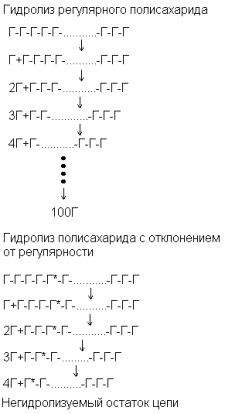
Г-свободная глюкоза или ее остаток, связанный «нормальной» для данного фермента связью; Г* - «аномальный» остаток, глюкозидная связь которого не расщепляется ферментом.
Поскольку мы не знаем, в каком месте располагается аномальное звено, примем в первом приближении, что оно с равной вероятностью может оказаться в любом положении. Тогда при одном аномальном звене на молекулу (неопределенность метилирования) ферментативный гидролиз будет останавливаться в среднем в середине каждой цепи. Это означает, что выход образующейся глюкозы составит 50% от общего содержания в образце. Такое расхождение с результатами, ожидаемыми для регулярного полисахарида (100%), можно обнаружить даже самыми грубыми методами анализа. Реальная же точность определения глюкозы стандартными методами составляет несколько процентов. Скажем осторожно, 5%. Это значит, что, если при ферментативном гидролизе такого полисахарида мы получаем глюкозу с количественным выходом, то с учетом 5%-й погрешности мы вправе утверждать, что по крайней мере 90% всех полимерных молекул в образце имеют регулярное строение и не содержат аномальных звеньев. Таким образом, применительно к нашему примеру регулярность, установленная методом метилирования, на дает даже права утверждать, что в полисахариде есть молекулы, не содержащие ни одного аномального звена, а регулярность, установленная с использованием ферментативного гидролиза, позволяет сказать, что не менее 90% всех молекул образца регулярны в строгом смысле слова. Разница количественная, но явно переходящая в качественную.
Может показаться, что ферментативный гидролиз является идеальным методом исследования структуры полисахаридов, обеспечивающим исчерпывающую информацию обо всех уровнях организации макромолекулы – от подробной характеристики мономерного звена до структуры всей конструкции в целом. Это действительно так, но только для тех полисахаридов, для которых доступны (и, что не менее важно, хорошо изучены) наборы соответствующих ферментов. А это можно сказать далеко не обо всех типах полисахаридов. Чтобы понять, почему это так, надо совершить маленький экскурс в биологию.
Ферменты продуцируются живыми организмами. Организм синтезирует ферменты, расщепляющие определенный тип полисахарида, если встречается с этим полисахаридом в естественных условиях и если расщепление такого полисахарида необходимо для его жизнедеятельности. Например, разветвленные глюканы типа амилопектина и гликогена почти универсально распространены в наземных растениях (амилопектин) и в животных организмах (гликоген) в качестве главного энергетического резерва. Для реализации этого резерва сами организмы нуждаются в соответствующих гидролитических ферментах. В не меньшей степени в таких ферментах нуждаются другие организмы – те, которые их поедают. Очевидно, например, что травоядные должны продуцировать ферменты, расщепляющие амилопектин (один из двух компонентов крахмала). Неудивительно поэтому, что такие ферменты можно выделить из многих доступных источников. Если же учесть большое значение, которое имеют такие ферменты для человека (и как ферменты собственно человеческого организма, и как важнейшие элементы биохимии сельскохозяйственных растений, и как активные участники многих процессов в пищевой промышленности и т.д.), то становится понятным, почему ферменты, расщепляющие гликоген и амилопектин, относятся к числу наиболее доступных и подробно изученных. Поэтому, в частности, именно в структурных исследованиях полисахаридов типа амилопектина и гликогена гидролитические ферменты являются сейчас основным инструментом, используя который удается почти исчерпывающе охарактеризовать их весьма сложные структуры.
Противоположным примером могут служить многие полисахариды водорослей, которые специфичны для этих растений и не встречаются в наземной флоре и фауне. Наивно было бы пытаться найти в наземных организмах расщепляющие их ферменты – этим организмам такие ферменты просто не нужны. Значит, источники подходящих полисахаридаз нужно искать в море, скорее всего среди травоядных морских животных. Вероятно, даже человеку, весьма далекому от биологии, понятно, что совсем не одно и то же – иметь источником фермента обычную лабораторную крысу или проростки картофеля, или пользоваться для этой цели, к примеру, морскими моллюсками, да еще не какими-нибудь вообще, а моллюсками определенного вида, обитающими в определенных районах и на определенных глубинах мирового океана. Чаще всего оказывается, что не только биохимия подходящего организма – продуцента нужного фермента – не изучена, но даже определить-то его как биологический вид может лишь считанное число специалиситов во всем мире. И тем не менее использование ферментов является по-видимому, одним из основных и уж конечно наиболее плодотворных путей подробной характеристики структур полисахаридов. Только путь этот устлан далеко не розами.
Так что же мы можем?
Мы рассказали о важнейших принципах и методах исследования структуры полисахаридов. Некоторые из них позволяют узнать о ближнем порядке моносахаридных остатков в цепи, другие дают сведения о дальнем порядке. Есть методы, пригодные лишь для изучения отдельных типов полисахаридов; есть и такие, область применения которых гораздо шире. К сожалению, среди них нет ни одного общего метода, который можно было бы использовать для изучения любого полисахарида (или хотя бы большинства из них), и нет ни одного метода, применение которого давало бы разумную степень уверенности в том, что с его помощью будет установлена полная структура полисахаридной молекулы. Нельзя даже сформулировать какое-то общее правило, следуя которому исследователь мог бы уверенно идти к цели в каждом новом случае: применяйте, например, такие-то и такие-то методы в такой-то последовательности, и вы сможете расшифровать полную структуру вашего полисахарида. Тем не менее строение множества полисахаридов известно сейчас с достаточной точностью и степенью подробности, причем нет оснований полагать, что эти структуры будут когда-либо опровергнуты. Возникает несколько парадоксальная ситуация: общих и надежных методов установления строения вроде бы нет, а структуры есть. Парадокс не устраняется каким-то простым способом, вопрос сложен и требует специального обсуждения.
Прежде всего, хотя известные методы структурного исследования действительно носят частный характер, почти для каждого типа полисахаридов можно подобрать комбинацию приемов и методов, достаточно информативных для конкретного случая. Совокупность сведений, полученных различными независимыми путями позволяет охарактеризовать структуру уже достаточно полно: получить довольно подробные данные о ближнем порядке звеньев, об общем плане построения молекулы, о многих элментах дальнего порядка. В то же время даже применение всех мыслимых методов исследования обеспечивает сейчас лишь ограниченные возможности точной локализации всех моносахаридных остатков в цепях. Кроме того, любой известный метод структурного анализа дает максимальную информацию только для «удачных» с точки зрения его принципа систем. Так, например, агароза устроена исключительно выгодно для успешного применения частичного гидролиза, а глюкан овса на редкость «хорошо приспособлен» для анализа его структуры с помощью деградации по Смиту. Такие «выгодные» структры встречаются, разумеется, далеко не всегда или, говоря более точно, не для всякого типа структуры можно подобрать столь эффективный метод исследования. Существо возникающих трудностей не сводится, однако, к ограниченности методического арсенала или к техническому несовершенству имеющихся методов. Гораздо более принципиальный характер носят следующие обстоятельства.
Если не считать отдельных случаев гидролиза экзополисахаридазами, у нас пока нет возможностей перебрать полисахаридную цепь звено за звеном, выяснив тем самым полную и точную последовательность всех остатков. А деструктивные методы типа частичного гидролиза оставляют возможность для существования каких-то минорных невыявленных сегментов (как мы видели на примере агарозы). Поэтому структуры цепей, выведенные на основании даже очень подробного исследования, как правило, характеризуются некоторой неопределенностью, по крайней мере в отношении наличия (или отсутствия) какого-то числа отклонений, аномальных звеньев, а также в отношении ограниченной точности определения количественных параметров структуры (таких, например, как число разветвлений на макромолекулу). Расширение арсенала методов, примененных к данному полисахариду, и повышение их точности может, конечно, снизить верхнюю оценку для содержания миноров и для ошибки в определении количественных параметров, однако не сможет устранить неопределенность полностью. В этом смысле процесс установления строения полисахарида и последующего уточнения его структуры есть асимптотическое приближение к недостижимой истине, тогда как надежно установленная ковалентная структура типичного низкомолекулярного соединения или такого биополимера, как белок, представляет собой истину «в последней инстанции», которая далее уже не может быть уточнена или поколеблена.
Другое обстоятельство, еще более фундаментального характера, позволяет поставить под сомнение целесообразность особо точного определения полисахаридных структур. Вспомним то, что говорилось о микрогетерогенности полисахаридных цепей. Благодаря этому явлению, в образце полисахарида, обычно содержится множество близко родственных структур. Поэтому локализация отдельных моносахаридных звеньев в цепях может быть достигнута с точностью, по крайней мере не большей, чем вариации структур молекул внутри образца, связанные с микрогетерогенностью. Принципиально можно, конечно, свести к минимуму структурные вариации такого типа, например, при помощи тех или иных химических или ферментативных обработок (вспомним, как был превращен нерегулярный полисахарид порфиран в производное регулярного полисахарида агарозы) и путем особо прецизионного фракционирования. Для таких полисахаридов со сведенным к минимуму разбросом структурных параметров можно, по крайней мере, в принципе, установить строение гораздо более точно.
Вопрос, однако, в том, что, собственно, будет отражать такая структура. Она не только не отвечает характеристикам биополимера в том виде, в каком он функционирует в живой клетке, но даже неспособна характеризовать каждый компонент смеси, составляющей реальный биополимер. Более того, значительные вариации структурных характеристик полисахаридных цепей существуют, по-видимому, и для различных представителей данного биологического вида, и для различных клеток одного многоклеточного организма, и для данного организма или данной клетки на разных стадиях развития или различных условиях существования. В этом смысле на углеводные биополимеры закон постоянства состава не распространяется.
Поэтому не исключено, что для понимания химических основ функционирования углеводсодержащих биополимеров в живых системах важны скорее несколько огрубленные, усредненные сведения о структуре, т.е. именно те, которые получаются при использовании современных методов исследования этих объектов. С другой стороны, для изучения микрогетерогенности как явления, понимания его биологического смысла и биосинтетических причин как раз важным кажется именно прецизионное, особо точное определение строения отдельных компонентов тех сложных смесей, какими являются такие биополимеры. Так что в столь сложном вопросе, как стратегия структурных исследований полисахаридов, оба, казалось бы взаимоисключающих, ответа на вопрос о целесообразной точности и глубине проникновения в материал оказываются правильными.
Так все-таки, способна или неспособна современная наука справляться со структурами сложных полисахаридов? Могут ли они быть установлены точно? В какой мере можно доверять структурам, фигурирующим в литературе в качестве известных?
Вопрос резонный, и обсуждается он вполне серьезно в профессиональных дискуссиях, хотя далеко не в столь прямолинейной форме. При этом высказываемые оценки расходятся довольно широко – от весьма оптимистических до весьма пессимистических. Авторы этой книги, хотя и имеют по этому вопросу определенное мнение, обязаны быть объективными и не навязывать свое мнение читателю. Поэтому мы попробуем изложить крайние точки зрения, акцентируя внимание на спорных моментах и не стремясь найти какой-то единственно правильный ответ. Вспомним поучительные слова лауреата Нобелевской премии профессора Роберта Робинсона: «Вообще-то, разница между наукой и религией заключается вот в чем: наука твердит, что, возможно, ошибается, тогда как религия утверждает, что наверняка права». Итак, суммируем основные доводы «за» и «против» возможности современной науки определять структуры полисахаридных цепей.
Аргументы «за». То, что говорилось о несовершенсте современных методов об ограниченности областей их применения, о трудностях определения дальнего порядка в полисахаридных цепях, конечно, справедливо. Нельзя, однако, забывать о резком расширении возможностей наших методов при их совместном применении. Информация при этом не складывается арифметически, а скорее умножается. Вот, например, одна из таких схем. Частичный кислотный или ферментативный гидролиз удаляет боковые цепи. Из данных мономерного анализа и состава продуктов гидролиза можно рассчитать моносахаридный состав и длину боковых цепей. Остаток – главная цепь – устроен значительно проще, и для его анализа пригодны уже многие методы. Теперь тот же полисахарид подвергают деградации по Смиту, которая в благоприятном случае приводит к расщеплению главной цепи. Мы получаем, так сказать, две неполные карты структуры в разных красках. А их наложение друг на друга даст уже полную картину, потому что неопределенности различных путей не совпадают. И подобных комбинаций разных методов возможно множество, так что для большинства полисахаридов удается уже сейчас собрать почти исчерпывающую структурную информацию. Так что при достаточной настойчивости и изобретательности мы сможем расшифровать структуру любого полисахарида.
Возражение. Тем не менее, сколько бы мы ни уточняли структуру, всегда остается возможность где-то вставить один-два неучтенных моносахаридных звена, а то и целый сегмент, и такая структура будет приводить к тому же набору экспериментальных данных. Даже в самых простых случаях линейных регулярных полисахаридов можно предположить малого числа аномальных звеньев, которые остались незамеченными из-за ограниченной чувствительности аналитики. Так что в принципе мы вправе поставить под сомнение надежность почти всех известных полисахаридных структур, в том числе и тех, которые уже фигурируют в учебниках и считаются окончательными.
Контраргументы. Такой скепсиси носит слишком уж отвлеченный характер. Следует отталкиваться от живой практики. Достаточно посмотреть, как много сложнейших структур уже расшифровано, особенно в последние годы. Может быть, тот или иной конкретный вывод и удалось бы поколебать или даже опровергнуть. Но в целом картина вырисовывается логичная и внутренне непротиворечивая. По мере накопления данных полисахариды удается все увереннее объединять в определенные классы с характерными типами структур, общие закономерности их композиции проглядываются все более отчетливо. А это подтверждает надежность каждого отдельного вывода. Характерный пример – О-антигенные цепи бактериальных липополисахаридов. Среди них многие ксеротипы имеют главную цепь регулярного строения, в которой повторяющимся звеном служит небольшой олигосахаридный фрагмент. И каждый новый представитель этого класса, структура которого становится известной, подтверждает это обобщение. А механизм биосинтеза этих полисахаридов, который был недавно установлен, позволяет понять, как такая регулярность возникает, и почему все эти полисахариды должны иметь именно регулярное строение. Так что структура каждого из этих биополимеров, взятая изолированно, возможно, и может быть поставлена под сомнение, однако в целом система знаний о данной группе полисахаридов оказывается весьма и весьма надежной и устойчивой.
Возражение: Не следует, однако, переоценивать значение таких обобщений. Иной раз трудно даже сказать, чего от них больше: пользы или вреда. Вспомним, как такие концепции появляются. Устанавливают строение нескольких первых, простейших представителей некоторого класса полисахаридов. Именно простейших (по той причине, что работа над ними приходит к концу раньше). Так как об этом классе еще ничего не известно, над структурами работают очень тщательно. И выясняется, что эти полисахариды регулярны (с теми, впрочем, оговорками, которые уже высказывались).
Рождается смелая гипотеза (именно гипотеза!) о том, что так же построены и другие полисахариды этого типа. Работа со следующими представителями идет уже легче: путеводной нитью служит гипотеза о регулярности; исследователи знают, что именно они должны найти: регулярную структуру. И, конечно, они ее находят. Даже подтверждают достаточно надежно, хотя иной раз уже не столь надежно, как для первых таких полисахаридов.
Дальше идет, что называется, «вал»: все новым и новым полисахаридам этого класса смелее и смелее (а значит, с меньшими основаниями) приписывают ожидаемый тип структуры. А потом мы бегло просматриваем литературу и видим, что структуры всех изученных полисахаридов этого класса прекрасно вписываются в общую схему. И уверенно говорим о надежной системе знаний. А более внимательный взгляд покажет, что эта система базируется лишь на очень небольшом числе действительно подробно и максимально надежно охарактеризованных структур. И живет такая схема, кочует из книги в книгу, из обзора в обзор как нечто общепринятое, пока жизнь властно не заставит пересмотреть ее. И приходится заново перепроверять множество структур, а многое и опровергать.
Контраргумент. Но здесь уже есть преувеличение. Конечно, некоторая тенденция к переоценке таких удобных обобщений действительно существует. Но на самом деле выводы о типе структуры внутри класса строятся не на единичных примерах. Скорее уж ненадежные и сомнительные структуры единичны. Так что оснований для типизации полисахаридных структур бывает достаточно.
Возражение. Нельзя, однако, рассуждать по принципу: «если большинство, то и все». Математик сказал бы, что тут нет достаточных данных для полной индукции. Обобщать можно и нужно, но не следует забывать, что вывод о регулярности всех полисахаридов данного класса есть всего лишь гипотеза, а не закон природы. Так что будь то десятый или сотый представитель этого класса, к установлению его строения нужно относиться столь же ответственно и критично, как к установлению строения первого, и делать утверждение о регулярности можно лишь тогда, когда для этого есть прямые экспериментальные основания, а не аналогии с другими сходными полисахаридами.
Контраргумент. Но ведь так чаще всего и бывает. В конце концов, в большинстве работ авторы не утверждают ничего большего, чем им позволяет прямой эксперимент. И их выводы о структуре можно уточнить, но нельзя опровергнуть.
Возражение. Однако это не есть законченные четкие структуры. В любой из них найдется ряд усредненных, округленных, приближенных параметров. И о каждом, даже очень хорошо изученном, полисахариде остается еще узнать очень многое
Контраргумент. Тем не менее это максимум того, что можно сейчас сделать. И это совсем не мало. В конце концов, отражают наши структурные данные объективную реальность? Отражают! Позволяют на структурном, молекулярном, уровне показать и объяснить разницу между различными полисахаридами? Позволяют! Дают основу для первых суждений о связи структуры и функции? В значительной мере дают. Так давайте же примем ту степень приближения, которая нам сейчас доступна.
На такой формуле, вероятно, и следует остановиться: полисахаридные структуры приближенны, и в этом надо отдавать себе ясный отчет; но это та максимальная степень приближения к истине, которая достигается современными методами. Методы же исследования полисахаридных структур необходимо еще совершенствовать и, что важнее, создать принципиально новые, которые позволили бы решить проблему миноров, подойти к вопросу о дальнем порядке звеньев в нерегулярных полисахаридах, словом, ответить на те вопросы, решение которых нам пока недоступно. Что же касается аргументов «за» и «против», то они не столько опровергают, сколько дополняют друг друга. Приведенную аргументацию нельзя отнести к тем или иным спорящим научным школам или отдельным личностям. Она отражает, скорее, разные грани одной области науки, или, еще вернее, разные состояния одного и того же Исследователя.


