Гидратация
Гидратация (от греч. hydor — вода), процессы связывания воды химическими веществами. Различают несколько видов гидратации.
Гидратация окислов приводит к гидроокисям, представляющим собой щёлочи, кислоты или амфотерные соединения. Так, присоединение воды к окиси кальция даёт гидроокись кальция (в технике этот процесс называется «гашение извести»):
СаО + H2O = Ca (OH)2.
Гидратация серного ангидрида в промышленности чают серную кислоту, а окислов азота — азотную кислоту:
SO2 + H2O = H2SO4,
3NO2 + H2O = 2HNO3 + NO.
При гидратации трёхокиси мышьяка образуется слабая мышьяковистая кислота, имеющая амфотерные свойства:
As2O3 + 3H2O = 2H3AsO3.
Гидратация органических соединений происходит по кратным связям; в случае циклических соединений гидратация приводит к раскрытию циклов. Обычно эти реакции происходят в присутствии щелочей, кислот или гетерогенных катализаторов (каталитическая гидратация). Гидратация этого типа играет огромную роль в препаративной органической химии и промышленности органического синтеза. Так, в результате прямой гидратации олефинов получают спирты, например этиловый спирт из этилена:
CH2 = CH2 + H2O ® CH3CH2OH.
Гидратация ацетилена приводит к ацетальдегиду (реакция Кучерова) (промежуточный продукт — неустойчивый виниловый спирт):
CH º CH + H2O ® [СН2=СН—ОН] ® CH3CHO.
В результате гидратации кетена образуется уксусная кислота, а окиси этилена — этиленгликоль:
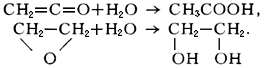
В перечисленных примерах вода реагирует таким образом, что происходит разрыв связи между атомом водорода и группой OH.
Многие неорганические и некоторые органические вещества образуют с водой твёрдые кристаллогидраты, постоянного состава, которые ведут себя как индивидуальные химические соединения. Так, безводный сульфат меди CuSO4 бесцветен; из его водных растворов кристаллизуется ярко-синий гидрат CuSO4·5H2O — медный купорос, при нагревании которого образуется сначала голубой CuSO4·3H2O, затем CuSO4·H2O белого цвета; при 258°С соль полностью обезвоживается. К этому же типу относится гидратация молекул в растворах с образованием гидратов различного состава, находящихся в равновесии друг с другом и водой; например, при растворении спирта образуются гидраты с 3,4 и 8 молекулами H2O. При растворении электролитов происходит гидратация ионов, затрудняющая ассоциацию последних. Энергия гидратации в значительной степени компенсирует энергию диссоциации электролита; т. о., гидратация ионов является одной из главных причин электролитической диссоциации в водных растворах. Образование кристаллогидратов и гидратация молекул и ионов в растворах являются частными случаями сольватации, т. е. присоединения молекул растворителя. К гидратации относят также процессы, приводящие к связыванию воды за счёт адсорбционных сил (см. Адсорбция). См. также Вода.
В биологических системах при гидратации происходит присоединение (связывание) воды различными субстратами организма. Вода, входящая в образующиеся при гидратации гидратные оболочки, составляет основное количество т. н. связанной воды протоплазмы клетки. С гидратацией связаны многие биологические процессы. Так, гидратация ионов влияет на их проникновение в клетку, а гидратация белков изменяет некоторые их свойства — в частности ферментативную активность.
Процесс, обратный гидратации, т. е. потеря связанной веществами воды, называется дегидратацией. Гидратация и дегидратация постоянно происходят в процессах обмена веществ, в частности обмена воды, в организмах.
