Тантал (хим. элемент)
Тантал (латинское Tantalum), Та, химический элемент V группы периодической системы Менделеева; атомный номер 73, атомная масса 180,948; металл серого цвета со слегка свинцовым оттенком. В природе находится в виде двух изотопов: стабильного 181Та (99,99%) и радиоактивного 180Та (0,012%; Т1/2= 1012 лет). Из искусственно полученных радиоактивный 182Та (Т1/2 = 115,1 сут) используют как радиоактивный индикатор.
Элемент открыт в 1802 шведским химиком А. Г. Экебергом; назван по имени героя древнегреческой мифологии Тантала (из-за трудностей получения тантала в чистом виде). Пластичный металлический тантал впервые получил в 1903 немецкий химик В. Больтон.
Распространение в природе. Среднее содержание тантала в земной коре (кларк)2,5×10-4% по массе. Характерный элемент гранитной и осадочной оболочек (среднее содержание достигает 3,5×10-4%); в глубинных частях земной коры и особенно в верхней мантии тантала мало (в ультраосновных породах 1,8×10-6%). В большинстве магматических пород и биосфере тантал рассеян; его содержание в гидросфере и организмах не установлено. Известно 17 собственных минералов тантала и более 60 танталсодержащих минералов; все они образовались в связи с магматической деятельностью (танталит, колумбит, лопарит, пирохлор и др.). В минералах тантал находится совместно с ниобием вследствие сходства их физических и химических свойств (см. Танталовые руды и Ниобиевые руды). Руды тантала известны в пегматитах гранитных и щелочных пород, карбонатитах, в гидротермальных жилах, а также в россыпях, которые имеют наибольшее практическое значение.
Физические и химические свойства. Тантал имеет кубическую объёмно-центрированную решётку (а = 3,296 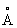 ); атомный радиус 1,46
); атомный радиус 1,46 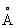 , ионные радиусы Та2+ 0,88 А, Та5+ 0,66 А; плотность 16,6 г/см3 при 20 °С; tпл 2996 °С; tкип 5300 °С; удельная теплоёмкость при 0—100 °С 0,142 кдж/(кг×К) [0,034 кал/(г × °С)]; теплопроводность при 20—100 °С 54,47 вт/(м×К) [0,13 кал/ (см ×сек ×°С)]. Температурный коэффициент линейного расширения 8,0×10-6 (20—1500 °С); удельное электросопротивление при 0°С 13,2×10-8 ом×м, при 2000 °С 87×10-8 ом×м. При 4,38 К становится сверхпроводником. Тантал парамагнитен, удельная магнитная восприимчивость 0,849×10-6 (18 °С). Чистый тантал — пластичный металл, обрабатывается давлением на холоду без значительного наклёпа. Его можно деформировать со степенью обжатия 99% без промежуточного отжига. Переход тантала из пластичного в хрупкое состояние при охлаждении до -196 °С не обнаружен. Модуль упругости тантала 190 Гн/м2 (190×102 кгс/мм2) при 25 °С. Предел прочности при растяжении отожжённого тантала высокой чистоты 206 Мн/м2 (20,6 кгс/мм2) при 27 °С и 190 Мн/м2 (19 кгс/мм2) при 490 °С; относительное удлинение 36% (27 °С) и 20% (490 °С). Твёрдость по Бринеллю чистого рекристаллизованного тантала 500 Мн/м2 (50 кгс/мм2). Свойства тантала в большой степени зависят от его чистоты; примеси водорода, азота, кислорода и углерода делают металл хрупким.
, ионные радиусы Та2+ 0,88 А, Та5+ 0,66 А; плотность 16,6 г/см3 при 20 °С; tпл 2996 °С; tкип 5300 °С; удельная теплоёмкость при 0—100 °С 0,142 кдж/(кг×К) [0,034 кал/(г × °С)]; теплопроводность при 20—100 °С 54,47 вт/(м×К) [0,13 кал/ (см ×сек ×°С)]. Температурный коэффициент линейного расширения 8,0×10-6 (20—1500 °С); удельное электросопротивление при 0°С 13,2×10-8 ом×м, при 2000 °С 87×10-8 ом×м. При 4,38 К становится сверхпроводником. Тантал парамагнитен, удельная магнитная восприимчивость 0,849×10-6 (18 °С). Чистый тантал — пластичный металл, обрабатывается давлением на холоду без значительного наклёпа. Его можно деформировать со степенью обжатия 99% без промежуточного отжига. Переход тантала из пластичного в хрупкое состояние при охлаждении до -196 °С не обнаружен. Модуль упругости тантала 190 Гн/м2 (190×102 кгс/мм2) при 25 °С. Предел прочности при растяжении отожжённого тантала высокой чистоты 206 Мн/м2 (20,6 кгс/мм2) при 27 °С и 190 Мн/м2 (19 кгс/мм2) при 490 °С; относительное удлинение 36% (27 °С) и 20% (490 °С). Твёрдость по Бринеллю чистого рекристаллизованного тантала 500 Мн/м2 (50 кгс/мм2). Свойства тантала в большой степени зависят от его чистоты; примеси водорода, азота, кислорода и углерода делают металл хрупким.
Конфигурация внешних электронов атома Та 5d36s2. Наиболее характерная степень окисления тантала + 5; известны соединения с низшей степенью окисления (например, TaCl4, ТaClз, TaCl2), однако их образование для тантала менее характерно, чем для ниобия.
В химическом отношении тантал при обычных условиях малоактивен (сходен с ниобием). На воздухе чистый компактный тантал устойчив; окисляться начинает при 280 °С. Имеет лишь один стабильный окисел — пятиокись Ta2O5, которая существует в двух модификациях: a-форме белого цвета ниже 1320 °С и b-форме серого цвета выше 1320 °С; имеет кислотный характер. С водородом при температуре около 250 °С тантал образует твёрдый раствор, содержащий до 20 атомных % водорода при 20 °С; при этом тантал становится хрупким; при 800—1200 °С в высоком вакууме водород выделяется из металла и его пластичность восстанавливается. С азотом при температуре около 300 °С образует твёрдый раствор и нитриды Ta2N и TaN; в глубоком вакууме выше 2200 °С поглощённый азот вновь выделяется из металла. В системе Та — С при температуре до 2800 °С установлено существование трёх фаз: твёрдого раствора углерода в тантале, низшего карбида Т2С и высшего карбида TaC. Тантал реагирует с галогенами при температуре выше 250 °С (с фтором при комнатной температуре), образуя галогениды преимущественно типа TaX5 (где Х = F, Cl, Вг, I), При нагревании Та взаимодействует с С, В, Si, Р, Se, Те, водой, CO, CO2, NO, HCI, H2S.
Чистый тантал исключительно устойчив к действию многих жидких металлов: Na, К и их сплавов, Li, Pb и др., а также сплавов U — Mg и Pu — Mg. Тантал характеризуется чрезвычайно высокой коррозионной устойчивостью к действию большинства неорганических и органических кислот: азотной, соляной, серной, хлорной и др., царской водки, а также многих др. агрессивных сред. Действуют на тантал фтор, фтористый водород, плавиковая кислота и её смесь с азотной кислотой, растворы и расплавы щелочей. Известны соли танталовых кислот — танталаты общей формулы xMe2O×уТа2О5×Н2О: метатанталаты MeTaO3, ортотанталаты Me3TaO4, соли типа Me5TaO5, где Me — щелочной металл; в присутствии перекиси водорода образуются также пертанталаты. Наиболее важны танталаты щелочных металлов — KTaO3 и NaTaO3; эти соли — сегнетоэлектрики.
Получение. Руды, содержащие тантал, редки, комплексны, бедны танталом; перерабатывают руды, содержащие до сотых долей процента (Та, Nb)2O5, и шлаки восстановительной плавки оловянных концентратов. Основным сырьём для производства тантала, его сплавов и соединений служат танталитовые и лопаритовые концентраты, содержащие соответственно около 8% Ta2O5 и 60% и более Nb2O5. Концентраты перерабатывают обычно в три стадии: 1) вскрытие, 2) разделение Та и Nb и получение их чистых соединений, 3) восстановление и рафинирование Та. Танталитовые концентраты разлагают кислотами или щелочами, лопаритовые — хлорируют. Разделяют Та и Nb с получением чистых соединений экстракцией, например трибутилфосфатом из плавиково-кислых растворов, или ректификацией хлоридов.
Для производства металлического тантала применяют восстановление его из Ta2O5 сажей в одну или в две стадии (с предварительным получением TaC из смеси Ta2O5 с сажей в атмосфере CO или H2 при 1800—2000 °С); электрохимическое восстановление из расплавов, содержащих K2TaF7 и Ta2O3, и восстановление натрием K2TaF7 при нагревании. Возможны также процессы термической диссоциации хлорида или восстановление из него тантала водородом. Компактный металл производят либо вакуумной дуговой, электроннолучевой или плазменной плавкой, либо методами порошковой металлургии. Слитки или спечённые из порошков штабики обрабатывают давлением; монокристаллы особо чистого тантала получают бестигельной электроннолучевой зонной плавкой.
Применение. Тантал обладает комплексом ценных свойств — хорошей пластичностью, прочностью, свариваемостью, коррозионной устойчивостью при умеренных температурах, тугоплавкостью, низким давлением пара, высоким коэффициентом теплопередачи, небольшой работой выхода электронов, способностью образовывать анодную плёнку (Ta2O3) с особыми диэлектрическими характеристиками и «уживаться» с живой тканью организма. Благодаря этим свойствам тантал находит применение в электронике, химическом машиностроении, ядерной энергетике, в металлургии (производство жаропрочных сплавов, нержавеющих сталей), в медицине; в виде TaC его применяют в производстве твёрдых сплавов. Из чистого тантала изготовляют электрические конденсаторы для полупроводниковых приборов, детали электронных ламп, коррозионноустойчивую аппаратуру для химической промышленности, фильеры в производстве искусственного волокна, лабораторную посуду, тигли для плавки металлов (например, редкоземельных) и сплавов, нагреватели высокотемпературных печей; теплообменники для ядерно-энергетических систем. В хирургии листы, фольгу, проволоку из тантала применяют для скрепления костей, нервов, наложения швов и др. Применение находят танталовые сплавы и соединения.
Лит.: Зеликман А. Н., Меерсон Г. А., Металлургия редких металлов, М., 1973.,
О. П. Колчин.
