Цирконий
Цирконий (лат. Zirconium), Zr, химический элемент IV группы периодической системы Менделеева; атомный номер 40, атомная масса 91,22; серебристо-белый металл с характерным блеском. Известно пять природных изотопов циркония: 90Zr (51,46%), 91Zr (11,23%), 92Zr (17,11%) 94Zr (17,4%), 96Zr (2,8%). Из искусственных радиоактивных изотопов важнейший 95Zr (T1/2 = 65 сут); используется в качестве изотопного индикатора.
Историческая справка. В 1789 немецкий химик М. Г. Клапрот в результате анализа минерала циркона выделил двуокись циркония. Порошкообразный цирконий впервые был получен в 1824 И. Берцелиусом, а пластичный — в 1925 нидерландскими учёными А. ван Аркелом и И. де Буром при термической диссоциации иодидов циркония.
Распространение в природе. Среднее содержание циркония в земной коре (кларк) 1,7×10-2% по массе, в гранитах, песчаниках и глинах несколько больше (2×10-2%), чем в основных породах (1,3×10-2%). Максимальная концентрации циркония — в щелочных породах (5×10-2%). Цирконий слабо участвует в водной и биогенной миграции. В морской воде содержится 0,00005 мг/л циркония. Известно 27 минералов циркония; промышленное значение имеют бадделеит ZrO2, циркон. Основные типы месторождений циркония: щелочные породы с малаконом и цитролитом; магнетит-форстерит-апатитовые породы и карбонатиты с бадделеитом; прибрежно-морские и элювиально-делювиальные россыпи.
Физические и химические свойства. Цирконий существует в двух кристаллических модификациях: a-формы с гексагональной плотноупакованной решёткой (а = 3,228 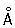 ; с = 5,120
; с = 5,120 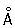 ) и b-формы с кубической объёмноцентрированной решёткой (а = 3,61
) и b-формы с кубической объёмноцентрированной решёткой (а = 3,61 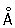 ). Переход a ® b происходит при 862 °C. Плотность a-циркония (20 °C) 6,45 г/см3; tпл 1825 ± 10 °C; tкип 3580—3700 °C; удельная теплоёмкость (25—100 °С) 0,291 кдж/(кг×К) [0,0693 кал/(г×°С)], коэффициент теплопроводности (50 °С) 20,96 вт/(м×К) [0,050 кал/(см×сек×°С)]; температурный коэффициент линейного расширения (20—400 °С) 6,9×10-6; удельное электрическое сопротивление циркония высокой степени чистоты (20°С) 44,1 мком×см. температура перехода в состояние сверхпроводимости 0,7 К. Цирконий парамагнитен; удельная магнитная восприимчивость увеличивается при нагревании и при —73 °С равна 1,28×10-6, а при 327 °С — 1,41×10-6. Сечение захвата тепловых нейтронов (0,18 ± 0,004)×10-28 м2, примесь гафния увеличивает это значение. Чистый цирконий пластичен, легко поддаётся холодной и горячей обработке (прокатке, ковке, штамповке). Наличие растворённых в металле малых количеств кислорода, азота, водорода и углерода (или соединений этих элементов с цирконием) вызывает хрупкость циркония. Модуль упругости (20 °С) 97 Гн/м2 (9700 кгс /мм2); предел прочности при растяжении 253 Мн/м2 (25,3 кгс/мм2); твёрдость по Бринеллю 640—670 Мн/м2 (64—67 кгс/мм2); на твёрдость очень сильное влияние оказывает содержание кислорода: при концентрации более 0,2% цирконий не поддаётся холодной обработке давлением.
). Переход a ® b происходит при 862 °C. Плотность a-циркония (20 °C) 6,45 г/см3; tпл 1825 ± 10 °C; tкип 3580—3700 °C; удельная теплоёмкость (25—100 °С) 0,291 кдж/(кг×К) [0,0693 кал/(г×°С)], коэффициент теплопроводности (50 °С) 20,96 вт/(м×К) [0,050 кал/(см×сек×°С)]; температурный коэффициент линейного расширения (20—400 °С) 6,9×10-6; удельное электрическое сопротивление циркония высокой степени чистоты (20°С) 44,1 мком×см. температура перехода в состояние сверхпроводимости 0,7 К. Цирконий парамагнитен; удельная магнитная восприимчивость увеличивается при нагревании и при —73 °С равна 1,28×10-6, а при 327 °С — 1,41×10-6. Сечение захвата тепловых нейтронов (0,18 ± 0,004)×10-28 м2, примесь гафния увеличивает это значение. Чистый цирконий пластичен, легко поддаётся холодной и горячей обработке (прокатке, ковке, штамповке). Наличие растворённых в металле малых количеств кислорода, азота, водорода и углерода (или соединений этих элементов с цирконием) вызывает хрупкость циркония. Модуль упругости (20 °С) 97 Гн/м2 (9700 кгс /мм2); предел прочности при растяжении 253 Мн/м2 (25,3 кгс/мм2); твёрдость по Бринеллю 640—670 Мн/м2 (64—67 кгс/мм2); на твёрдость очень сильное влияние оказывает содержание кислорода: при концентрации более 0,2% цирконий не поддаётся холодной обработке давлением.
Внешняя электронная конфигурация атома Zr 4d25s2. Для циркония характерна степень окисления +4. Более низкие степени окисления +2 и +3 известны для циркония только в его соединениях с хлором, бромом и йодом. Компактный цирконий медленно начинает окисляться в пределах 200—400 °С, покрываясь плёнкой циркония двуокиси ZrO2; выше 800 °С энергично взаимодействует с кислородом воздуха. Порошкообразный металл пирофорен — может воспламеняться на воздухе при обычной температуре. Цирконий активно поглощает водород уже при 300 °С, образуя твёрдый раствор и гидриды ZrH и ZrH2; при 1200—1300 °С в вакууме гидриды диссоциируют и весь водород может быть удалён из металла. С азотом цирконий образует при 700—800 °С нитрид ZrN. Цирконий взаимодействует с углеродом при температуре выше 900 °С с образованием карбида ZrC. Карбид и нитрид циркония — твёрдые тугоплавкие соединения; карбид циркония — полупродукт для получения ZrCl4. Цирконий вступает в реакцию с фтором при обычной температуре, а с хлором, бромом и иодом при температуре выше 200 °С, образуя высшие галогениды ZrX4 (где Х — галоген). Цирконий устойчив в воде и водяных парах до 300 °С, не реагирует с соляной и серной (до 50%) кислотами, а также с растворами щелочей (цирконий — единственный металл, стойкий в щелочах, содержащих аммиак). С азотной кислотой и царской водкой взаимодействует при температуре выше 100 °С. Растворяется в плавиковой и горячей концентрированной (выше 50%) серной кислотах. Из кислых растворов могут быть выделены соли соответствующих кислот разного состава, зависящего от концентрации кислоты. Так, из концентрированных сернокислых растворов циркония осаждается кристаллогидрат Zr (SO4)2×4H2O; из разбавленных растворов — основные сульфаты общей формулы xZrO2×ySO3×zH2O (где х: y > 1). Сульфаты циркония при 800—900 °С полностью разлагаются с образованием двуокиси циркония. Из азотнокислых растворов кристаллизуется Zr (NO3)4×5H2O или ZrO (NO3)2×xH2O (где х = 2—6), из солянокислых растворов — ZrOCl2×8H2O, который обезвоживается при 180—200 °С.
Получение. В СССР основным промышленным источником получения циркония является минерал циркон ZrSiO4. Циркониевые руды обогащаются гравитационными методами с очисткой концентратов магнитной и электростатической сепарацией. Металл получают из его соединений, для производства которых концентрат вначале разлагают. Для этого применяют: 1) хлорирование в присутствии угля при 900—1000 °С (иногда с предварительной карбидизацией при 1700—1800 °С для удаления основной части кремния в виде легколетучего SiO); при этом получается ZrCl4, который возгоняется и улавливается; 2) сплавление с едким натром при 500—600 °С или с содой при 1100 °С: ZrSiO4 + 2Na2CO3 = Na2ZrO3 + Na2SiO3 + 2CO2; 3) спекание с. известью или карбонатом кальция (с добавкой CaCl2) при 1100—1200 °С: ZrSiO4 + 3CaO = CaZrO3 + Ca2SiO4; 4) сплавление с фторосиликатом калия при 900 °С: ZrSiO4 + K2SiF6 = K2ZrF6 + 2SiO2. Из спёка или плава, полученного в случаях щелочного вскрытия (2,3), вначале удаляют соединения кремния выщелачиванием водой или разбавленной соляной к той, а затем остаток разлагают соляной или серной; при этом образуются соответственно оксихлорид и сульфаты. Фтороцирконатный спек (4) обрабатывают подкисленной водой при нагревании; при этом в раствор переходит фтороцирконат калия, 75—90% которого выделяется при охлаждении раствора.
Для выделения соединений циркония из кислых растворов применяют следующие способы: 1) кристаллизацию оксихлорида циркония ZrOCl2×8H2O при выпаривании солянокислых растворов; 2) гидролитическое осаждение основных сульфатов циркония xZrO2×ySO3(zH2O из сернокислых или солянокислых растворов; 3) кристаллизацию сульфата циркония Zr (SO4)2 при добавлении концентрированной серной кислоты или при выпаривании сернокислых растворов. В результате прокаливания сульфатов и хлоридов получают ZrO2.
Соединения циркония, полученные из рудного сырья, всегда содержат примесь гафния. Цирконий отделяют от этой примеси фракционной кристаллизацией K2ZrF6, экстракцией из кислых растворов органическими растворителями (например, трибутилфосфатом), ионообменными методами, избирательным восстановлением тетрахлоридов (ZrCl4 и HfCl4).
Цирконий в виде порошка или губки получают металлотермическим восстановлением ZrCl4, K2ZrF6 и ZrO2. Хлорид восстанавливают магнием или натрием, фтороцирконат калия — натрием, а двуокись циркония — кальцием или его гидридом. Электролитический порошкообразный цирконий получают из расплава смеси солей галогенидов циркония и хлоридов щелочных металлов. Компактный ковкий цирконий получают плавлением в вакуумных дуговых печах спрессованных губки или порошка, обычно служащих расходуемым электродом. Цирконий высокой степени чистоты производят электроннолучевой плавкой слитков, полученных в дуговых печах, или прутков после иодидного рафинирования.
Применение. Сплавы на основе циркония, очищенного от гафния, применяют преимущественно в качестве конструкционных материалов в ядерных реакторах, что обусловлено малым сечением захвата тепловых нейтронов (см. Циркониевые сплавы). Цирконий входит в состав ряда сплавов (на основе магния, титана, никеля, молибдена, ниобия и др. металлов), используемых как конструкционные материалы, например, для ракет и др. летательных аппаратов. Из сплавов циркония с ниобием делают обмотки магнитов сверхпроводящих. В литейном производстве применяют цирконистые огнеупоры. К числу наиболее распространённых пьезокерамических материалов (пьезокерамики) относится группа цирконата — титаната свинца (например, ЦТС-23). В металлокерамических материалах (керметах) металлическим составляющим является цирконий, а керамическим — его двуокись ZrO2. При производстве генераторных ламп проволока из циркония служит геттером.
Цирконий используют в качестве коррозионно-стойкого материала в химическом машиностроении. Присадки циркония служат для раскисления стали и удаления из неё азота и серы. Порошкообразный цирконий применяют в пиротехнике и в производстве боеприпасов. Сульфат циркония — дубитель в кожевенной промышленности.
Лит.: Справочник по редким металлам, ред. К. А. Гемпел, пер. с англ., М., 1965; Основы металлургии, т. 4, М., 1967; Зеликман А. Н., Меерсон Г. А., Металлургия редких металлов, М., 1973.
О. Е. Крейн.
