Имиды карболовых кислот
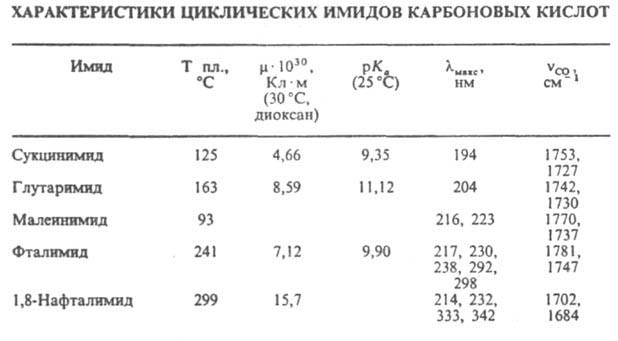
ИМИДЫ КАРБОНОВЫХ КИСЛОТ, соед., содержащие группу —С(О)—NH—С(О)—. Линейные имиды - производные монокарбоновых к-т, напр. (CH3CO)2NH; их называют также диациламидами. Наиб. значение имеют циклич. имиды (ф-ла I, где Z - opг. остаток) - производные дикарбоновых к-т, напр., сукцинимид. Имиды карбоновых к-т - кристаллич. в-ва. Их физ. св-ва представлены в таблице.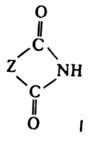
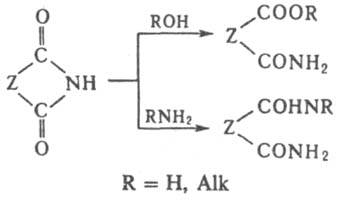
Они легко гидролизуются в кислой и щелочной средах до моноамидов дикарбоновых к-т (амидокислот). Алкоголиз приводит к амидоэфирам, аммонолиз и аминолиз - к диамидам:
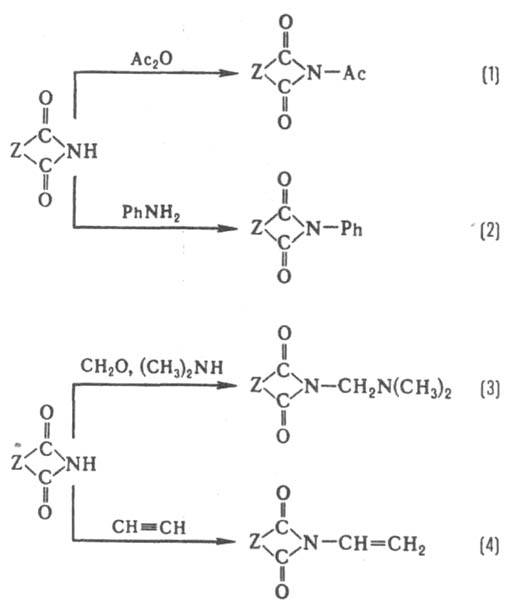
С основаниями имиды карбоновых кислот образуют соли, гидролизующиеся в воде, но устойчивые в спирте. Алкилирование К-соли фталимида алкилгалогенидами и послед. гидролиз - классич. метод синтеза первичных аминов (см. Габриеля реакция). В р-ции имидов карбоновых кислот с галогенами или гипогалогенитами образуются N-галогенимиды (напр., N-бромсукцинимид), применяемые в орг. синтезе как источники атомарного или положительно заряженного галогена. В присутствии оснований N-галогенимиды претерпевают перегруппировку Гофмана. Обработка фталимида щелочным гипохлоритом лежит в основе пром. метода получения антраниловой к-ты. При взаимодействии циклич. имидов карбоновых кислот с избытком NaNH2 образуется дианион, алкилирующийся по a-атому углерода, напр.:
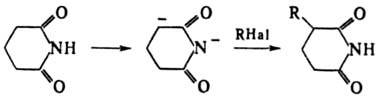
Имиды карбоновых кислот исключительно устойчивы к окислению, но легко восстанавливаются комплексными гидридами металлов, водородом в присут. катализаторов или электрохимически, причем циклические образуют, в зависимости от условий, a-гидроксилактамы, лактамы или амины. Линейные имиды карбоновых кислот получают ацилированием первичных или вторичных амидов ангидридами, галогенангидридами, изопропениловыми эфирами карбоновых к-т или кетенами. Циклич. имиды карбоновых кислот образуются при циклизации азотсодержащих производных дикарбоновых к-т - моноамидов, диамидов, эфироамидов, мононитрилов, напр.:
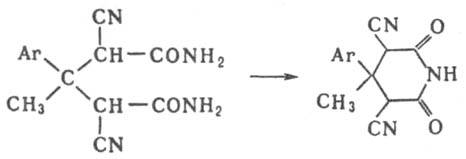
Имиды карбоновых кислот также синтезируют каталитич. окислит. аминированием углеводородов (напр., фталимид - из ксилола), окислением азотсодержащих гетероциклов (напр., сукцинимид - из пиррола), карбонилированием амидов b,g-ненасыщенных к-т в присут. Со(СО)8 (напр., глутаримид - из амида винилуксусной к-ты).
Анализ имидов карбоновых кислот основан на их превращ. в гидроксамовые к-ты и колориметрич. определении последних, а также на полярографич. восстановлении. Производные имидов карбоновых кислот- вулканизующие агенты, дисперсные красители и пигменты с высокой светопрочностью, регуляторы роста растений, фунгициды, бактерициды, лек. ср-ва. См. также Полиимиды.
Литература
Общая органическая химия, пер. с англ., т. 4, М., 1983, с. 388-536; Hargreaves М. К., Pritchard J. G., Dave H. R., "Chem. Rev.", 1970, v. 70, № 4, p. 439-69. Д. В. Иоффе.
Ещё по теме
Циклические имиды кислот — свойства и применение
Химические реакции аминокислот — механизмы и производные
Амиды кислот — свойства и применение
Активирование карбоксильной группы в химии пептидов
Этаноламиды жирных кислот — свойства и применение
Химические свойства амидов
Способы получения аминов
