Жидкостная хроматография
ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ, вид хроматографии, в к-рой подвижной фазой (элюентом) служит жидкость. Неподвижной фазой м. б. твердый сорбент, твердый носитель с нанесенной на его пов-сть жидкостью или гель. Различают колоночную жидкостную хроматографию, в к-рой через колонку, заполненную неподвижной фазой, пропускают порцию разделяемой смеси в-в в потоке элюента (под давлением или под действием силы тяжести), и тонкослойную жидкостную хроматографию (см. Тонкослойная хроматография), в к-рой элюент перемещается под действием капиллярных сил по плоскому слою сорбента, нанесенного на стеклянную пластинку или металлич. фольгу, вдоль пористой полимерной пленки, по пов-сти цилиндрич. кварцевой или керамич. палочки, по полоске хроматографич. бумаги (см. Хроматография на бумаге). Разработан также метод тонкослойной жидкостной хроматографии под давлением (элюент прокачивают через слой сорбента, зажатого между пластинами). Жидкостная хроматография применяется как аналитическая и препаративная (см. Хроматография препаративная). В высокоэффективной жидкостной хроматографии (ВЭЖХ) используют колонки диаметром до 5 мм, плотно упакованные сорбентом с частицами малого размера (3-10 мкм); давление для прокачивания элюента до 3.107 Па (ее называют также хроматографией высокого давления). Варианты ВЭЖХ -микроколоночная хроматография на наполненных колонках малого диаметра и капиллярная хроматография на полых и наполненных сорбентом капиллярных колонках. К жидкостной хроматографии обычно относят также гидродинамич. хроматографию, где неподвижная фаза отсутствует. В этом случае используют тот факт, что скорость потока элюента максимальна в центре полого капилляра и минимальна у его стенок, а разделяемые компоненты распределяются между движущимися с разной скоростью слоями элюента в соответствии со своими размерами или под влиянием наложенного в поперечном направлении внеш. силового поля (центробежного, электрического, магнитного).Основные виды. По механизму удерживания разделяемых в-в неподвижной фазой жидкостная хроматография делится на осадочную хроматографию, адсорбционную, распределительную, ионообменную хроматографию (в т. ч. ионную хроматографию), ион-парную, лигандообменную хроматографию, эксклюзионную хроматографию (ситовую) и аффинную хроматографию (биоспецифическую). Осадочная жидкостная хроматография основана на разл. р-римости осадков, образующихся при взаимод. компонентов анализируемой смеси с реагентом-осадителем. Преимущества метода в том, что получающиеся вдоль сорбента зоны имеют резкие границы, содержат осадки только одного в-ва и часто разделены зонами чистого сорбента. Метод пока не нашел широкого распространения. Адсорбционная жидкостная хроматография в зависимости от относит. полярности сорбента и элюента подразделяется на нормально-фазную и обращенно-фазную. В первом случае адсорбция в-в происходит на полярном сорбенте [напр., силикагеле, содержащем гидроксильные (силанольные) группы] из неполярного элюента благодаря донорно-акцепторному взаимод. или образованию водородных связей. Во втором - на пов-сти гидрофобизир. сорбента из полярного элюента благодаря дисперсионному (гидрофобному) взаимод. разделяемых молекул с пов-стью (образование водородной связи возможно в подвижной фазе с молекулами элюента, к-рый, как правило, содержит воду). В распределительной жидкостной хроматографии разделение основано на распределении в-в между двумя жидкими фазами: неподвижной, нанесенной на пов-сть носителя, и подвижной элюентом. В зависимости от полярности жидких фаз возможны нормально-фазный и обращeнно-фазный варианты. В первом случае на пов-сть или в поры пористого носителя наносится полярная жидкость, не смешивающаяся с неполярным элюентом, во втором - используется нсполярная неподвижная фаза и полярный элюент. К распределительной жидкостной хроматографии относится и экстракционная жидкостная хроматография, в к-рой неподвижной фазой служит орг. экстрагент, нанесенный на твердый носитель, а подвижной - водный р-р разделяемых соединений. В качестве экстрагентов используют диалкилфосфорные и алкилсульфоновые к-ты, фенолы (кислотные экстрагенты), триалкилфосфаты, фосфиноксиды и др. (нейтральные экстрагенты), амины, четвертичные аммониевые основания, а также серосодержащие фосфорорг. соед., хелатообразующие реагенты и др. Применяется для разделения и концентрирования неорг. соед., напр., ионов щелочных металлов, актиноидов, РЗЭ и др. близких по св-вам элементов, в процессах переработки отработанного ядерного горючего. В ионообменной жидкостной хроматографии разделение основано на разл. способности разделяемых ионов к р-ции ионного обмена с фиксир. ионами сорбента, образующимися в результате диссоциации ионогенных групп последнего. В зависимости от знака заряда фиксир. ионов различают катиониты (закреплен анион) и аниониты (закреплен катион) (см. Иониты). Разделение ионов регулируют подбором оптим. значений рН элюента и его ионной силы. Вариант ионообменной жидкостной хроматографии - ионная хроматография, в к-рой разделенные анионы (катионы) детектируют в виде к-т (соотв. оснований) высокочувствит. кондуктометрическим детектором, а высокоэффективные колонки наполнены поверхностно-активным ионитом с небольшой емкостью. Ион-парную жидкостную хроматографию можно рассматривать как комбинацию адсорбционной и ионообменной; в качестве неподвижной фазы используют гидрофобизир. адсорбент, а подвижной - водно-орг. элюент с добавлением поверхностно-активных ионогенных соед. (ион-парных реагентов), напр., додецилсульфата Na или триметилцетиламмоний бромида. Разделение основано на удерживании ион-парного реагента на гидрофобной пов-сти адсорбента с образованием ионита, к-рый и проводит разделение ионогенных соединений. Возможно также образование ионных пар разделяемых ионов с ион-парным реагентом, к-рые затем удерживаются на гидрофобизир. пов-сти адсорбента. Лигандообменная жидкостная хроматография основана на разл. способности разделяемых соед. образовывать комплексы с катионами переходных металлов - Cu(II), Ni(II), Zn(II), Cd(II), Co(II) и др. - и фиксир. группами (лигандами) неподвижной фазы. Часть координац. сферы ионов металла занята молекулами воды или др. слабыми лигандами, к-рые могут вытесняться молекулами разделяемых соединений. Наиб. эффективна для разделения оптич. изомеров. Аффинная жидкостная хроматография основана на образовании прочной связи со специфич. группами неподвижной фазы (лигандами, аффинантами). Взаимод. лигандов с разделяемыми в-вами основано на биол. ф-ции последних. Так, при разделении ферментов лигандами служат их субстраты, ингибиторы или коферменты, токсинов - рецепторы, белков - антитела и т. д. Особенно эффективна в биотехнологии и биомедицине для выделения ферментов, белков, гормонов. В эксклюзионной (ситовой, гель-проникающей, гель-фильтрационной) жидкостной хроматографии разделение основано на различиях в размерах молекул; молекулы малых размеров проникают в сравнительно тонкие поры сорбента и задерживаются в них, крупные молекулы либо не проникают в поры, либо проникают лишь в широкие поры и проходят колонку с незначит. удерживанием. Пов-сть сорбента и состав элюента подбирают так, чтобы исключить или уменьшить энергию адсорбц. взаимодействия (однако иногда при разделении олигомеров удобнее использовать адсорбц. механизм). Применяют для разделения олигомеров и полимеров (в т. ч. биологических).
Основные хроматографические величины и их определение. При разделении в-в с помощью жидкостной хроматографии могут применяться проявительный, фронтальный и вытеснительный варианты. Чаще всего используют проявительный вариант, при к-ром в колонку в потоке элюента вводят порцию разделяемой смеси. Выход компонентов смеси из колонки регистрируется на хроматограмме в виде пиков (рис., а). Из хроматограммы определяют времена удерживания несорбирующегося (t0) и разделенных компонентов (tR1 , tR2 и т. д.) и ширину оснований пиков (tw1, tw2 и т. д.). Зная объемную скорость элюента w, вычисляют: мертвый объем колонки Vm = t0.w; исправленный удерживаемый объем компонента V'R = (tR — t0)w = t'Rw, где t'R - исправленное время удерживания компонента; коэф. емкости колонки по отношению к данному компоненту k' = (tR - t0)/t0 = V'R/Vm; эффективность колонки (характеризуется числом эквивалентных теоретич. тарелок) N = 16(tR/tw)2; коэф. селективности a = t'R2 /t'R1 = V'R2/V'R1 = k'2/k'1 и разрешение RS = 2(tR2 - tR1)/(tw1 + tw2). Высота или площадь пиков характеризует концентрацию компонентов, а удерживаемые объемы - качеств. состав смеси. Идентификацию компонентов обычно проводят по совпадению времен удерживания со стандартными в-вами; используют также физ.-хим. или хим. методы.
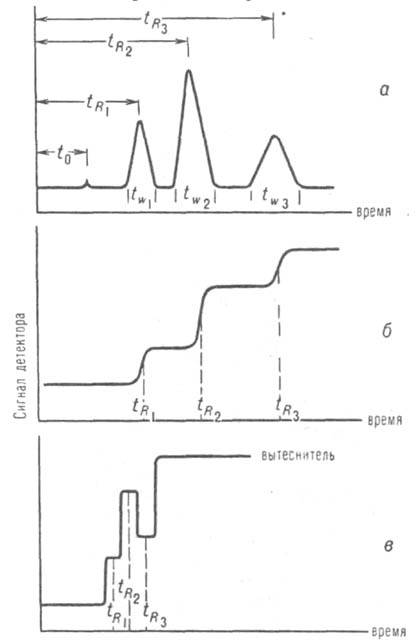
Варианты жидкостной хроматографии: а)проявительный; б)фронтальный; в) вытеснительный.
При фронтальном варианте через колонку непрерывно пропускают смесь разделяемых в-в, к-рая играет роль подвижной фазы. Хроматограмма в этом случае представляет собой ступени, высоты к-рых пропорциональны концентрациям компонентов; удерживаемые объемы определяют по времени удерживания компонентов (рис., б). При дифференцировании такой хроматограммы получают картину, как в проявит. варианте. В вытеснит. варианте компоненты смеси, введенной в колонку, вытесняются элюентом, к-рый адсорбируется сильнее любого компонента. Порядок выхода компонентов определяется силой взаимод. их с пов-стью сорбента (рис., в). Главный показатель, характеризующий жидкостную хроматографию, - разрешение RS двух в-в, к-рое связано с осн. хроматографич. величинами соотношением:
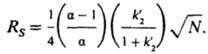
Коэф. емкости k' существенно влияет на величину RS: при изменении k' от 0 до 10 (оптим. пределы) RS сильно возрастает. Значение k' определяется уд. пов-стью сорбента и его кол-вом в колонке, а также константой адсорбц. равновесия (константой Генри). Коэф. селективности a определяется различием констант адсорбц. равновесия двух разделяемых компонентов. При увеличении a (от 1 до ~ 5) RS резко возрастает, при дальнейшем увеличении a - меняется мало Селективность колонок зависит от хим. структуры пов-сти (в эксклюзионной хроматографии - геом. структуры) сорбента, состава элюента, т-ры колонки и строения разделяемых соединений. Т. к. сорбция хроматографируемых в-в в жидкостной хроматографии определяется попарным взаимод. трех осн. компонентов системы - сорбента, разделяемых в-в и элюента, то изменение состава элюента - удобный способ оптимизации процесса разделения. Эффективность колонки зависит от размера частиц и структуры пор адсорбента, от равномерности набивки колонки, вязкости элюента и скорости массообмена. Удлинение колонки не всегда приводит к улучшению разделения, т. к. возрастает сопротивление колонки, увеличивается давление элюента на входе и время проведения опыта, снижается чувствительность и точность анализа из-за уширения пика анализируемого компонента. При RS / 1 пики двух в-в на хроматограмме разделяются практически полностью, с ростом RS увеличивается время разделения; при RS < 1 - разделение неудовлетворительное. В препаративной хроматографии в связи с введением сравнительно больших кол-в разделяемых в-в колонка работает с перегрузкой. При этом снижается коэф. емкости, возрастает высота, эквивалентная теоретич. тарелке, что приводит к уменьшению разрешения.
Адсорбенты. Осн. адсорбент - кремнезем (силикагель), гидроксилированный или химически модифицированный; используют также Аl2О3, углеродные адсорбенты, полимеры, содержащие ионогенные, комплексообразующие группы или группы, способные к специфич. взаимод. с биологически активными в-вами. Размер частиц силикагеля в аналит. колонках 3-10 мкм, в препаративных - 20-70 мкм. Малый размер частиц увеличивает скорость массообмена и повышает эффективность колонки. Совр. аналит. колонки длиной 10-25 см, заполненные силикагелем с размером частиц 5 мкм, позволяют разделить сложные смеси из 20-30 компонентов. При уменьшении размера частиц до 3-5 мкм возрастает эффективность колонки, но и растет ее сопротивление и для достижения скорости потока элюента 0,5-2,0 мл/мин требуется давление (1-3).107Па. Силикагель выдерживает такой перепад давления, гранулы же полимерных сорбентов более эластичны и деформируются. В последнее время разработаны механически прочные густосетчатые полимерные сорбенты макропористой структуры, приближающиеся по своей эффективности к силикагелям. Форма частиц сорбента размером 10 мкм и выше не оказывает большого влияния на эффективность колонки, однако предпочитают сферич. сорбенты, к-рые дают более проницаемую упаковку. Внутр. структура частицы силикагеля представляет собой систему сообщающихся каналов. Для жидкостной хроматографии используют сорбенты с диаметром пор 6-25 нм и уд. пов-стью 600-100 м2/г. Разделение в жидкостной хроматографии проводят в осн. на силикагелях, модифицир. р-цией алкил- и арилхлорсиланов или алкилэтоксисиланов с силанольными группами пов-сти. С помощью таких р-ций прививают группы С8Н17, С18Н37 или С6Н5 (для получения сорбентов с гидрофобизир. пов-стью), g-аминопропильные, нитрильные, гидроксильные (в диольных сорбентах) группы и др. Сорбенты с гидрофобизир. пов-стью углеродной природы получают также пиролизом орг. соед. на пов-сти силикагеля. В ион-парной, лигандообменной и адсорбц. хроматографиях используют метод динамич. адсорбц. модифицирования, при к-ром в элюент вводят незначит. добавки адсорбирующегося на пов-сти адсорбента соед., содержащего функц. группу, к-рая обеспечивает желаемый механизм разделения, напр., при разделении углеводов на гидроксилир. силикагеле в элюент добавляют пиперазин. Возможна также постоянная адсорбц. модификация пов-сти желаемым реагентом при использовании элюента, не смывающего последний.
Элюенты должны элюировать анализируемые соед. с оптим. значениями k', обладать низкой вязкостью, обеспечивать необходимый уровень селективности, быть дешевыми, нетоксичными, инертными, совместимыми с методами детектирования (напр., с УФ детектором нельзя использовать в качестве элюента бензол). В нормально-фазной хроматографии обычно используют углеводороды (гексан, гептан, изооктан, циклогексан) с добавлением небольших кол-в СНСl3, изо-С3Н7ОН, диизопропилового эфира; в обращенно-фазной смесь воды с CH3CN, СН3ОН, С2Н5ОН, диоксаном, ТГФ, ДМФА. Если компоненты разделяемой смеси имеют близкие значения k', хроматографируют одним элюентом (изократич. режим), если отдельные компоненты смеси сильно удерживаются сорбентом, используют серию элюентов возрастающей силы (ступенчатое или непрерывное градиентное элюирование).
Аппаратура. Совр. жидкостной хроматограф включает емкости для элюентов, насосы высокого давления, дозатор, хроматографич. колонку, детектор, регистрирующий прибор, систему управления и мат. обработки результатов. Элюенты подаются в насос через фильтр, задерживающий пылевые частицы (больше 0,2 мкм); иногда через элюенты пропускают небольшой ток гелия для удаления растворенного воздуха и предотвращения образования пузырьков в детекторе (особенно в случае водных и полярных элюентов). В аналит. хроматографах для подачи элюента в колонку используют поршневые насосы с системой обратной связи, позволяющие сглаживать пульсацию потока в пределах 1-2% и обеспечивать объемные скорости от 0,1 до 25 мл/мин при давлении до ~ 3.107 Па. В микроколоночной хроматографии объемные скорости потока элюента ниже: 10-1000 мкл/мин. В случае градиентного элюирования используют неск. насосов, к-рые управляются программатором и подают в камеру смешения 2-3 компонента элюента, оставляя постоянной общую скорость потока. Для введения пробы в колонку, находящуюся под большим давлением, без остановки потока используют спец. микродозирующие краны, связанные с петлей известного объема для исследуемой пробы р-ра. Разработаны дозировочные системы с автоматич. отбором и вводом пробы с помощью микродозирующих кранов или шприцов. Колонки для ВЭЖХ изготовляют чаще всего из нержавеющей стальной полированной трубки длиной 10-25 см и внутр. диаметром 3-5 мм. Используют также стеклянные колонки, помещенные в металлич. кожух; в микроколоночной хроматографии - набивные металлич. колонки с внутр. диаметром 1,0-1,5 мм, набивные стеклянные микроколонки диаметром 70-150 мкм и полые капиллярные колонки диаметром 10-100 мкм; в препаративной - колонки диаметром от 2 до 10 см и более. Для равномерного и плотного заполнения колонок сорбентом используют суспензионный метод набивки. Суспензию готовят из сорбента и подходящей орг. жидкости, к-рая подается под давлением до 5.107 Па в колонку. Для определения выходящих из колонки разделенных компонентов используют детекторы (см. Детекторы хроматографические). Для увеличения чувствительности детектора иногда применяют послеколоночную дериватизацию компонентов смеси. Для этого с потоком элюента вводят такие реагенты, к-рые, взаимодействуя с разделенными в-вами, образуют производные с более выраженными св-вами, напр., сильнее поглощают в УФ или видимой области спектра или обладают большей флуоресцирующей способностью и т. д. Иногда дериватизацию проводят до хроматографич. анализа и разделяют производные, а не исходные в-ва. Регистрацию хроматограмм и обработку данных проводят с помощью самописца или мини-ЭВМ, к-рая также рассчитывает количеств. характеристики и, в нек-рых случаях, качеств. состав смесей. Микропроцессор обеспечивает автоматич. ввод пробы, изменение по заданной программе состава элюента при градиентном элюировании, поддержание т-ры колонки.
Применение. Жидкостная хроматография важнейший физ.-хим. метод исследования в химии, биологии, биохимии, медицине, биотехнологии. Ее используют для анализа, разделения, очистки и выделения аминокислот, пептидов, белков, ферментов, вирусов, нуклеотидов, нуклеиновых к-т, углеводов, липидов, гормонов и т. д.; изучения процессов метаболизма в живых организмах лек. препаратов; диагностики в медицине; анализа продуктов хим. и нефтехим. синтеза, полупродуктов, красителей, топлив, смазок, нефтей, сточных вод; изучения изотерм сорбции из р-ра, кинетики и селективности хим. процессов. В химии высокомол. соед. и в произ-ве полимеров с помощью жидкостной хроматографии анализируют качество мономеров, изучают молекулярно-массовое распределение и распределение по типам функциональности олигомеров и полимеров, что необходимо для контроля продукции. Жидкостную хроматографию используют также в парфюмерии, пищ. пром-сти, для анализа загрязнений окружающей среды, в криминалистике. Хроматография как метод разделения в-в предложена М. С. Цветом в 1903 на примере жидкостной хроматографии. Литература
