Металлы
Металлы, простые вещества, обладающие в обычных условиях характерными свойствами: высокой электропроводностью и теплопроводностью, отрицательным температурным коэффициентом электропроводности, способностью хорошо отражать электромагнитные волны (блеск и непрозрачность), пластичностью. Металлы в твёрдом состоянии имеют кристаллическое строение. В парообразном состоянии металлы одноатомны.
Перечисленные выше характерные свойства металлов обусловлены их электронным строением. Атомы металлов легко отдают внешние (валентные) электроны. В кристаллической решётке металлов не все электроны связаны со своими атомами. Некоторая их часть (~ 1 на атом) подвижна. Эти электроны могут более или менее свободно перемещаться по металлам. Существование свободных электронов (электронов проводимости) в металлах объясняется зонной теорией (см. Твёрдое тело). Металлы можно представить себе в виде остова из положительных ионов, погруженного в «электронный газ». Последний компенсирует силы электростатического отталкивания между положительными ионами и тем самым связывает их в твёрдое тело (металлическая связь).
Из известных (1974) 105 химических элементов 83 — металлы и лишь 22 — неметаллы. Если в длинном или «полудлинном» варианте периодической системы элементов Менделеева провести прямую линию от бора до астата (табл. 1), то можно считать, что неметаллы расположены на этой линии и справа от неё, а металлы — слева.
Не следует, однако, абсолютизировать ни свойства, характерные для металлов, ни их отличия от неметаллов. Металлический блеск присущ только компактным металлическим образцам. Тончайшие листки Ag и Au (толщиной 10-4 мм) просвечивают голубовато-зелёным цветом. Мельчайшие порошки металлов часто имеют чёрный или черно-серый цвет. Некоторые металлы (Zn, Sb, Bi) при комнатной температуре хрупки и становятся пластичными только при нагревании.
Вся совокупность перечисленных выше свойств присуща типичным металлам (например, Cu, Au, Ag, Fe) при обычных условиях (атмосферном давлении, комнатной температуре). При очень высоких давлениях (~ 105—106 ам) свойства металлов могут существенно измениться, а неметаллы приобрести металлические свойства.
Многие простые вещества по одним свойствам можно отнести к металлам, по др. — к неметаллам. Особенно много такого рода «нарушений» имеет место вблизи границы, проведённой в табл. 1. Так, Ge по внешнему виду — металл, в химическом отношении проявляет себя скорее как металл (легче отдаёт электроны, чем принимает), а по величине и характеру электропроводности Ge — полупроводник. Сурьма Sb имеет электросопротивление слишком большое для металла, однако температурный коэффициент сопротивления у Sb положительный и большой, как у металла; по способности отдавать электроны Sb также относится к металлам. As, Sb и Bi иногда называют полуметаллами. Po по внешнему виду — металл, в химическом отношении ему присущи свойства и металла, и неметалла — наряду с положительной валентностью (точнее окислительным числом) проявляется и отрицательная (— 2).
Металлические сплавы по свойствам имеют много общего с металлами, поэтому в физической, технической и экономической литературе нередко к металлам относят также и сплавы.
Историческая справка. Термин «металл» произошёл от греческого слова métallon (от metalléuo — выкапываю, добываю из земли), которое означало первоначально копи, рудники (в этом смысле оно встречается у Геродота, 5 в. до н. э.). То, что добывалось в рудниках, Платон называл metalléia. В древности и в средние века считалось, что существует только 7 металлов: золото, серебро, медь, олово, свинец, железо, ртуть (см. Знаки химические). По алхимическим представлениям, металлы зарождались в земных недрах под влиянием лучей планет и постепенно крайне медленно совершенствовались, превращаясь в серебро и золото (см. Алхимия). Алхимики полагали, что металлы — вещества сложные, состоящие из «начала металличности» (ртути) и «начала горючести» (серы). В начале 18 в. получила распространение гипотеза, согласно которой металлы состоят из земли и «начала горючести» — флогистона. М. В. Ломоносов насчитывал 6 металлов (Au, Ag, Cu, Sn, Fe, Pb) и определял металлы как «светлое тело, которое ковать можно». В конце 18 в. А. Л. Лавуазье опроверг гипотезу флогистона и показал, что металлы — простые вещества. В 1789 Лавуазье в руководстве по химии дал список простых веществ, в который включил все известные тогда 17 металлов (Sb, Ag, As, Bi, Со, Cu, Sn, Fe, Mn, Hg, Mo, Ni, Au, Pt, Pb, W, Zn). По мере развития методов химического исследования число известных металлов возрастало. В 1-й половине 19 в. были открыты спутники Pt, получены путём электролиза некоторые щелочные и щёлочноземельные металлы, положено начало разделению редкоземельных металлов, открыты неизвестные металлы при химическом анализе минералов. В 1860—63 методом спектрального анализа были открыты Cs, Rb, Tl, In. Блестяще подтвердилось существование металлов, предсказанных Д. И. Менделеевым на основе его периодического закона. Открытие радиоактивности в конце 19 в. повлекло за собой поиски природных радиоактивных металлов, увенчавшиеся полным успехом. Наконец, методом ядерных превращений начиная с середины 20 в. были искусственно получены радиоактивные металлы, в частности трансурановые элементы.
В конце 19 — начале 20 вв. получила физико-химическую основу металлургия — наука о производстве металлов из природного сырья. Тогда же началось исследование свойств металлов и их сплавов в зависимости от состава и строения (см. Металловедение, Металлофизика).
Химические свойства. В соответствии с местом, занимаемым в периодической системе элементов (табл. 1), различают металлы главных и побочных подгрупп. Металлы главных подгрупп (подгруппы а) называют также непереходными. Эти металлы характеризуются тем, что в их атомах происходит последовательное заполнение s- и р-электронных оболочек. В атомах металлов побочных подгрупп (подгруппы б), называют переходными, происходит достраивание d- и f-оболочек, в соответствии с чем их делят на d-группу и две f-группы — лантаноиды и актиноиды. В подгруппы а входят 22 металла: Li, Na, К, Rb, Cs, Fr (I a); Be, Mg, Ca, Sr, Ba, Ra (II a); Al, Ga, In, Tl (III a); Ge, Sn, Pb (IV a); Sb, Bi (V a); Po (VI а). В подгруппы б входят: 1) 33 переходных металла d-группы [Cu, Ag, Au (I б), Zn, Cd, Hg (II б); Sc, Y, La, Ac (III б); Ti, Zr, Hf, Ku (IV б); V, Nb, Ta, элемент с Z = 105 (V б), Cr, Mo, W (VI б), Mn, Te, Re (VII б), Fe, Co, Ni, Ru, Rh, Pd, 0s, lr, Pt (VIII б)]; 2) 28 металлов f-группы (14лантаноидов и 14 актиноидов).
Электронная структура атомов некоторых d-элементов имеет ту особенность, что один из электронов внешнего уровня переходит на d-подуровень. Это происходит при достройке этого подуровня до 5 или 10 электронов. Поэтому электронная структура валентных подуровней атомов d-элементов, находящихся в одной подгруппе, не всегда одинакова. Например, Cr и Mo (подгруппа VI б) имеют внешнюю электронную структуру соответственно 3d54s1 и 4d55s1, тогда как у W она 5d46s2. В атоме Pd (подгруппа VIII б) два внешних электрона «перешли» на соседний валентный подуровень, и для атома Pd наблюдается d10 вместо ожидаемого d8s2.
Металлам присущи многие общие химические свойства, обусловленные слабой связью валентных электронов с ядром атома: образование положительно заряженных ионов (катионов), проявление положительной валентности (окислительного числа), образование основных окислов и гидроокисей, замещение водорода в кислотах и т.д. Металлические свойства элементов можно сравнить, сопоставляя их электроотрицательность [способность атомов в молекулах (в ковалентной связи) притягивать электроны, выражена в условных единицах]; элементу присущи свойства металла тем больше, чем ниже его электроотрицательность (чем сильнее выражен электроположительный характер).
В периодической системе элементов Менделеева (табл. 1) в пределах каждого периода, начиная со 2-го, с увеличением атомного номера электроотрицательность возрастает от 2 до 7, начиная со щелочного металла и кончая галогеном (переход от металлов к неметаллам). В пределах подгрупп (а и б) с увеличением атомного номера электроотрицательность в общем уменьшается, хотя и не всегда последовательно. В семействах лантаноидов и актиноидов она сохраняется примерно на одном уровне.
Если расположить металлы в последовательности увеличения их нормальных потенциалов, получим т. н. ряд напряжений или ряд активностей (табл. 2 и 3). Рассмотрение этого ряда показывает, что по мере приближения к его концу — от щелочных и щёлочноземельных металлов к Pt и Au — электроположительный характер членов ряда уменьшается. Металлы от Li по Na вытесняют H2 из H2O на холоду, а от Mg по Tl — при нагревании. Все металлы, стоящие в ряду выше H2, вытесняют его из разбавленных кислот (на холоду или при нагревании). Металлы, стоящие ниже H2, растворяются только в кислородных кислотах (таких, как концентрированная H2SO4 при нагревании или HNO3), а Pt, Au — только в царской водке (Ir нерастворим и в ней).
Металлы от Li по Na легко реагируют с O2 на холоду; последующие члены ряда соединяются с O2 только при нагревании, а lr, Pt, Au в прямое взаимодействие с O2 не вступают.
Окислы металлов от Li по Al (табл. 2) и от La по Zn (табл. 3) трудно восстановимы; по мере продвижения к концу ряда восстановимость окислов увеличивается, а окислы последних его членов разлагаются на металлы и O2 уже при слабом нагревании. О прочности соединений металлов с кислородом (и др. неметаллами) можно судить и по разности их электроотрицательностей (табл. 1): чем она больше, тем прочнее соединение.
Табл. 2. — Нормальные электродные потенциалы непереходных металлов
| Система | Нормальный потенциал при 25 °С, в | Система | Нормальный потенциал при 25 °C, в | Система | Нормальный потенциал при 25 °С, в |
| Li Û Li+ + е | -3,0245 | Mg Û Mg2+ + 2е | -2,375 | Sn Û Sn2+ + 2e | -0,140 |
| Cs Û Cs+ + e | -3,020 | Be Û Be2+ + 2e | -1,69 | Pb Û Pb2+ + 2e | -0,126 |
| Rb Û Rb+ + e | -2,990 | Al Û Al3+ + 3e | -1,67 | Ha Û 2H+ + 2e | 0 |
| К Û K+ + e | -2,925 | Ga Û Ga3+ + 3e | -0,52 | Sb Û Sb3+ + 3e | +0,20 |
| Ra Û Ra2+ + 2е | -2,92 | Ga Û Ga2+ + 2e | -0,45 | Bi Û Bi3+ + 3e | +0,23 |
| Ba Û Ba2+ + 2e | -2,90 | In Û ln3++ 3e | -0,34 | Po Û Po3+ + 3e | +0,56 |
| Sr Û Sr2+ + 2e | -2,89 | Tl Û Tl++ е | -0,338 | Po Û Po2+ + 2е | +0,65 |
| Ca Û Ca2+ + 2e | -2,87 | In Û ln2+ + 2e | -0,25 | Tl Û Tl3+ + 3e | +0,71 |
| Na Û Na+ + е | -2,714 |
|
| Pb Û Pb4+ + 4е | +0,80 |
Табл. 3. — Нормальные электродные потенциалы переходных металлов
| Система | Потенциал при 25 °С, в | Система | Потенциал при 25 °C, в | Система | Потенциал при 25 °C, e |
| Ac Û Ac3+ + 3e | -2,60 | Cr Û Cr3+ + 3е | -0,74 | Ru Û Ru2+ + 2e | +0,45 |
| La Û La3+ + 3e | -2,52 | Fe Û Fe2+ + 2e | -0,44 | Mn Û Mn3+ + 3e | +0,47 |
| Y Û Y3+ + 3e | -2,37 | Cd Û Cd2+ + 2e | -0,402 | Cu Û Cu+ + e | +0,522 |
| Sc Û Sc3+ + 3e | -2,08 | Re Û Re3+ + 3e | -0,3 | Rh Û Rh2+ + 2e | +0,60 |
| Hf Û Hf4+ + 4е | -1,70 | Co Û Co2+ + 2e | -0,277 | W Û W6+ + 6e | +0,68 |
| Ti Û Ti3+ + 3е | -1,63 | Ni Û Ni2+ + 2е | -0,25 | Rh Û Rh3+ + 3e | +0,70 |
| Zr Û Zr4+ + 4е | -1,56 | Те Û Te2+ + 2e | -0,24 | 0s Û Os2+ + 2e | +0,70 |
| V Û V2+ + 2e | -1,18 | Mo Û Mo3+ + 3е | -0,20 | Ag Û Ag+++с | +0,779 |
| Mn Û Mn2++ 2e | -1,18 | H2 Û 2H+ + 2e | 0,000 | Pd Û Pd2+ + 2e | +0,83 |
| Nb Û Nb3+ + 3e | -1,10 | Fe Û Fe3+ + 3e | +0,036 | Hg Û Hg2+ + 2e | +0,854 |
| V Û V3+ +3e | -0,87 | W Û W3+ + 3e | +0,11 | lr Û lr3+ + 3e | +1,0 |
| Cr Û Cr2+ + 2e | -0,86 | Cu Û Cu2+ + 2e | +0,346 | Pt Û Pt2+ + 2e | +1,2 |
| Zn Û Zi3+ + 2e | -0,761 | Co Û Co3+ + 3e | +0,40 | Au Û Au3+ + 3e | +1,5 |
|
|
|
|
| Au Û Au+ + e | +1,7 |
Валентности (точнее, окислительные числа) непереходных металлов равны: +1 для подгруппы I а; +2 для II a; +1 и +3 для III a; +2 и +4 для IV a; +2, +3 и +5 для V a; — 2, +2, +4, +6 для VI a. У переходных металлов наблюдается ещё большее разнообразие окислительных чисел: +1, +2, +3 для подгруппы I б, +2 для II б; +3 для III б; +2, +3, +4 для IV б; +2, +3, +4, +5 для V б; +2, +3, +4, +5, +6 для VI б, +2, +3, +4, +5, +6, +7 для VII б, от +2 до +8 в VIII б. В семействе лантаноидов наблюдаются окислительные числа +2, +3 и +4, в семействе актиноидов — от +3 до +6. Низшие окислы металлов обладают основными свойствами, высшие являются ангидридами кислот (см. Кислоты и основания). Металлы, имеющие переменную валентность (например, Cr, Mn, Fe), в соединениях, отвечающих низшим степеням окисления [Cr (+2), Mn (+2), Fe (+2)], проявляют восстановительные свойства; в высших степенях окисления те же металлы [Cr (+6), Mn (+7), Fe (+3)] обнаруживают окислительные свойства. О химических соединениях металлов друг с другом см. в ст. Металлиды, о соединениях металлов с неметаллами см. в статьях Бориды, Гидриды, Карбиды, Нитриды, Окислы и др.
Лит.: Некрасов Б. В., Основы общей химии, 2 изд., т. 1—3, М., 1969—70; Дей М. К., Селбин Дж., Теоретическая неорганическая химия, пер. с англ., 2 изд., М., 1971; Барнард А., Теоретические основы неорганической химии, пер. с англ., М., 1968; Рипан Р., Четяну И., Неорганическая химия, т. 1—2, Химия металлов, пер. с рум., М., 1971—72. См. также лит. при ст. Неорганическая химия.
С. А. Погодин.
Физические свойства. Большинство металлов кристаллизуется в относительно простых структурах — кубических (кубические объёмноцентрированная ОЦК и гранецентрированная ГЦК решётки) и гексагональных ПГУ, соответствующих наиболее плотной упаковке атомов. Лишь небольшое число металлов имеет более сложные типы кристаллических решёток. Многие металлы в зависимости от внешних условий (температуры, давления) могут существовать в виде двух или более кристаллических модификаций (см. Полиморфизм). Полиморфные превращения иногда связаны с потерей металлических свойств, например превращение белого олова (b-Sn) в серое (a-Sn).
Электрические свойства. Удельная электропроводность металлов при комнатной температуре s ~ 10-6—10-4 ом-1см-1 (табл. 1), тогда как у диэлектриков, например у серы, s ~ 10-17 ом-1см-1. Промежуточные значения s соответствуют полупроводникам. Характерным свойством металлов как проводников электрического тока является линейная зависимость между плотностью тока и напряжённостью приложенного электрического поля (Ома закон). Носителями тока в металлах являются электроны проводимости, обладающие высокой подвижностью. Согласно квантово-механическим представлениям, в идеальном кристалле электроны проводимости (при полном отсутствии тепловых колебаний кристаллической решётки) вообще не встречают сопротивления на своём пути. Существование у реальных металлов электросопротивления является результатом нарушения периодичности кристаллической решётки. Эти нарушения могут быть связаны как с тепловым движением атомов, так и с наличием примесных атомов, вакансий, дислокаций и др. дефектов в кристаллах. На тепловых колебаниях и дефектах (а также друг на друге) происходит рассеяние электронов. Мерой рассеяния служит длина свободного пробега — среднее расстояние l между двумя последовательными столкновениями электронов. Величина удельной электропроводности s связана с длиной свободного пробега l соотношением:
s = nel/pF, (1)
где n — концентрация электронов проводимости (~1022—1023 см-3), е — заряд электрона, pF = 2ph (3n/8p)1/3 — граничный фермиевский импульс (см. Ферми поверхность), h — Планка постоянная. Зависимость а или удельного электросопротивления р от температуры Т связана с зависимостью l от Т. При комнатных температурах в металлах l ~ 10-6 см.
При температурах, значительно превышающих Дебая температуру, сопротивление r обусловлено главным образом тепловыми колебаниями кристаллической решётки и возрастает с температурой линейно:
r = rост (1 + aТ). (2)
Постоянная a называется температурным коэффициентом электропроводности и имеет при температуре Т = 0 °C типичное значение a = 4×10-5 град--1. При более низких температурах, когда влиянием тепловых колебаний атомов на рассеяние электронов можно пренебречь, сопротивление практически перестаёт зависеть от температуры. Это предельное значение сопротивления называется остаточным. Величина rост характеризует концентрацию дефектов в решётке металлов. Удаётся получить столь чистые (сверхчистые) и свободные от дефектов металлы, что их остаточное сопротивление в 104—105 раз превышает сопротивление этих металлов в обычных условиях. Длина свободного пробега электронов в сверхчистых металлах l ~ 10-2 см. Теоретическое рассмотрение показывает, что при низких температурах формула для удельного электросопротивления имеет вид:
r=rост+АТ2+ВТ5 (3)
где А и В — величины, не зависящие от Т. Член BT5 связан с рассеянием электронов на тепловых колебаниях атомов, а член AT2 — со столкновениями электронов друг с другом и даёт заметный вклад в сопротивление лишь у некоторых металлов, например у Pt. Однако закономерность (3) выполняется лишь приближённо.
У некоторых металлов и металлидов при определённой температуре, называемой критической, наблюдается полное исчезновение сопротивления — переход в сверхпроводящее состояние (см. Сверхпроводимость). Критические температуры чистых металлов лежат в интервале от сотых долей К до 9 К (табл. 1).
Если металлический образец, по которому течёт ток, поместить в постоянное магнитное поле, то в металлах возникают явления, обусловленные искривлением траекторий электронов в магнитном поле в промежутке между столкновениями (гальваномагнитные явления). Среди них важное место занимают Холла эффект и изменение электросопротивления металлов в магнитном поле (магнетосопротивление). Влияние магнитного поля тем больше, чем больше длина свободного пробега l, т. е. чем ниже температура и чем меньше примесей в металлах. При комнатной температуре магнитное поле 107—105 э изменяет сопротивление металлов лишь на доли %. При T £ 4 К в сверхчистых металлах сопротивление может измениться во много раз. Зависимость электросопротивления металлов от внешнего магнитного поля существенно зависит от характера энергетического спектра электронов, в частности от формы поверхности ферми. У многих металлических монокристаллов (Au, Cu, Ag и др.) наблюдается сложная анизотропия сопротивления в магнитном поле.
В магнитных полях ~ 104—105 э и при низких температурах у всех металлических монокристаллов наблюдается осциллирующая зависимость электросопротивления от магнитного поля (Шубникова — де Хааза эффект). Это явление — следствие квантования движения электронов в плоскости, перпендикулярной направлению магнитного поля. Как правило, квантовая осциллирующая зависимость в виде небольшой «ряби» наложена на обычную зависимость сопротивления от магнитного поля.
При нагревании металла до высоких температур наблюдается «испарение» электронов с поверхности металла (термоэлектронная эмиссия). Число электронов, вылетающих в единицу времени, определяется законом: n~exp (—j/kT), где k — Больцмана постоянная, j — работа выхода электронов из метаалы (см. Ричардсона формула). Величина j различна у разных металлов и зависит также от состояния поверхности. Эмиссия электронов с поверхности металла происходит также под действием сильных электрических полей ~107 в/см в результате туннельного просачивания электронов через сниженный полем потенциальный барьер (см. Туннельная эмиссия). В металлах наблюдаются явления фотоэлектронной эмиссии, вторичной электронной эмиссии и ионно-электронной эмиссии. Перепад температуры вызывает в металлах появление электрического тока или разности потенциалов (см. Термоэлектрические явления).
Тепловые свойства. Теплоёмкость металлов (табл. 1) обусловлена как ионным остовом (решёточная теплоёмкость Ср), так и электронным газом (электронная теплоёмкость Сэ). Хотя концентрация электронов проводимости в металлах очень велика (см. выше) и не зависит от температуры, электронная теплоёмкость мала и у большинства металлов наблюдается только при температурах ~ нескольких К. Возможность измерения Сэ связана с тем, что при уменьшении температуры Ср убывает пропорционально T3, а Сэ ~ Т. Для Cu: Сэ = 0,9×10-4RT, для Pd: Сэ = 1,6×10-3RT (R — газовая постоянная). Теплопроводность металлов осуществляется главным образом электронами проводимости. Поэтому между удельными коэффициентами электропроводности и теплопроводности существует простое соотношение, называемое Видемана — Франца законом.
Взаимодействие металлов с электромагнитными полями. Переменный электрический ток при достаточно высокой частоте течёт по поверхности металла, не проникая в его толщу (см. Скин-эффект). Электромагнитное поле частоты w проникает в металл лишь на глубину скин-слоя толщиной d.
Например, для Cu при (w = 108 гц d = 6×10-4 см. В таком слое поглощается незначительная часть электромагнитной энергии. Основная часть энергии переизлучается электронами проводимости и отражается (см. Металлооптика). В чистых металлах при низких температурах длина свободного пробега электронов l часто превышает глубину d. При этом напряжённость поля существенно изменяется на длине свободного пробега, что проявляется в характере отражения электромагнитных волн от поверхности металла (аномальный скин-эффект).
Сильное постоянное магнитное поле существенно влияет на электродинамические свойства металлов. В металлах, помещенных в такое поле, при условии, если частота электромагнитного поля кратна частоте прецессии электронов проводимости вокруг силовых линий постоянного магнитного поля, наблюдаются резонансные явления (см. Циклотронный резонанс). При определённых условиях в толще металла, находящегося в постоянном магнитном поле, могут распространяться слабо затухающие электромагнитные волны, т. е. исчезает скин-эффект. Электродинамические свойства металлов, помещенного в магнитное поле, сходны со свойствами плазмы в магнитном поле и являются одним из основных источников информации об электронах проводимости.
Для электромагнитных волн оптического диапазона металлы, как правило, практически непрозрачны и обладают характерным блеском (см. Отражение света, Зеркало). В поглощении света в видимом и ультрафиолетовом диапазонах некоторую роль играет внутренний фотоэффект. Отражение от поверхности металлов плоскополяризованного света, падающего под произвольным углом, сопровождается поворотом плоскости поляризации и появлением эллиптической поляризации (см. Вращение плоскости поляризации). Это явление используется для определения оптических констант металлов.
Общая структура характеристических рентгеновских спектров металлов и диэлектриков одинакова. Тонкая же структура линий, соответствующая квантовым переходам электронов из зоны проводимости на глубокие уровни, отражает распределение электронов проводимости по уровням энергии.
Магнитные свойства. Переходные металлы с недостроенными f- и d-электронными оболочками являются парамагнетиками. Некоторые из них при определённых температурах переходят в магнитоупорядоченное состояние (см. Магнетизм, Ферромагнетизм, Антиферромагнетизм, Кюри точка). Магнитное упорядочение существенно влияет на все свойства металлов, в частности на электрические свойства: в электросопротивление вносит вклад рассеяние электронов на колебаниях магнитных моментов. Гальваномагнитные явления при этом также приобретают специфические черты.
Магнитные свойства остальных металлов определяются электронами проводимости, которые вносят вклад в диамагнитную и парамагнитную восприимчивости металлов, и диамагнитной восприимчивостью ионного состава (см. Диамагнетизм, Парамагнетизм). Магнитная восприимчивость c большинства металлов относительно мала (c ~ 10-6) и слабо зависит от температуры.
При низких температурах Т и в больших магнитных полях Н ³ 104 kT у всех металлических монокристаллов наблюдается сложная осциллирующая зависимость суммарного магнитного момента от поля Н (см. Де Хааза — ван Альфена эффект), природа которого та же, что и у эффекта Шубникова — де Хааза. Исследование осцилляционных эффектов позволяет определить форму поверхности Ферми.
Механические свойства. Многие металлы обладают комплексом механических свойств, обеспечивающим их широкое применение в технике, в частности в качестве конструкционных материалов. Это, в первую очередь, сочетание высокой пластичности со значительной прочностью и сопротивлением деформации, причём соотношение этих свойств может регулироваться в большом диапазоне с помощью механической и термической обработки металлов, а также получением сплавов различного состава.
Исходной характеристикой механических свойств металлов является модуль упругости G, определяющий сопротивление кристаллической решётки упругому деформированию и непосредственно отражающий величину сил связи в кристалле. В монокристаллах эта величина, как и остальные механические характеристики, анизотропна и коррелирует с температурой плавления металла (например, средний модуль сдвига G изменяется от 0,18×1011 эрг/см3 для легкоплавкого Na до 27×1011 эрг/см3 для тугоплавкого Re).
Сопротивление разрушению или пластической деформации идеального кристалла ~ 10-1 G. Но в реальных кристаллах эти характеристики, как и все механические свойства, определяются наличием дефектов, в первую очередь дислокаций. Перемещение дислокаций по плотноупакованным плоскостям приводит к элементарному акту скольжения — основному механизму пластической деформации металлов. Др. механизмы двойникование и сбросообразование) существенны только при пониженных температурах. Важнейшая особенность металлов — малое сопротивление скольжению дислокации в бездефектном кристалле. Это сопротивление особенно мало в кристаллах с чисто металлической связью, которые обычно имеют плотноупакованные структуры (гранецентрированную кубическую или гексагональную). В металлах с ковалентной компонентой межатомной связью, имеющих объёмноцентрированную решётку, сопротивление скольжению несколько больше, однако всё же мало по сравнению с чисто ковалентными кристаллами. Сопротивление пластической деформации, по крайней мере в металлах с гранецентрированной кубической и гексагональной решётками, связано с взаимодействием движущихся дислокаций с др. дефектами в кристаллах, с др. дислокациями, примесными атомами, внутренними поверхностями раздела. Взаимодействие дефектов определяется искажениями решётки вблизи них и пропорционально G. Для отожжённых монокристаллов начальное сопротивление пластической деформации (предел текучести) обычно ~ 10-3—10-4 G. В процессе деформации число дислокаций в кристаллической решётке (плотность дислокаций b) увеличивается от 106—108 до 1012 см-2. Соответственно растет сопротивление пластической деформации 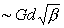 (d — межатомное расстояние). Это называют деформационным упрочнением или наклёпом. Для монокристаллов металлов характерно наличие трёх стадий деформационного упрочнения. На 1-й стадии значительная часть дислокаций выходит на поверхность и коэффициент упрочнения Q (коэффициент пропорциональности между напряжением и деформацией) мал; на 2-й стадии дислокации накапливаются в кристалле, их распределение становится существенно неоднородным: Q~G/300. На 3-й стадии b, G и Q уменьшаются вследствие аннигилляции дислокаций, выдавливаемых из их плоскостей скольжения. Значение этой стадии больше для металлов с объёмноцентрированной решёткой.
(d — межатомное расстояние). Это называют деформационным упрочнением или наклёпом. Для монокристаллов металлов характерно наличие трёх стадий деформационного упрочнения. На 1-й стадии значительная часть дислокаций выходит на поверхность и коэффициент упрочнения Q (коэффициент пропорциональности между напряжением и деформацией) мал; на 2-й стадии дислокации накапливаются в кристалле, их распределение становится существенно неоднородным: Q~G/300. На 3-й стадии b, G и Q уменьшаются вследствие аннигилляции дислокаций, выдавливаемых из их плоскостей скольжения. Значение этой стадии больше для металлов с объёмноцентрированной решёткой.
Степень «привязанности» дислокации к плоскости скольжения определяется шириной дислокации в этой плоскости, которая, в свою очередь, зависит от энергии g дефекта упаковки (величина g/Gd в металлах с гранецентрированной решёткой изменяется от 10-2 для Al, имеющего узкие дислокации, до 10-4 для сплавов Cu с широкими дислокациями). Процесс разрядки дислокационной плотности ускоряется при повышении температуры и может привести к релаксации и значительному восстановлению свойств кристаллов. Чем выше температура и меньше скорость деформирования, тем больше успевают развиться процессы релаксации и тем меньше деформационное упрочнение.
При Т > 0,5 Тпл в пластической деформации начинают играть существенную роль точечные дефекты, в первую очередь вакансии, которые, оседая на дислокациях, приводят к их выходу из плоскостей скольжения. Если этот процесс достаточно интенсивен, то деформация не сопровождается упрочнением: металл течёт с постоянной скоростью при неизменной нагрузке (ползучесть). Протекание процессов релаксации напряжений и постоянная разрядка дислокационной структуры обеспечивают высокую пластичность металлов при их горячей обработке, что позволяет придавать изделиям из металлов разнообразную форму. Отжиг сильно деформированных монокристаллов металлов нередко приводит к образованию поликристаллов с малой плотностью дислокаций внутри зёрен (рекристаллизация).
Достижимые степени деформации металлов ограничены процессом разрушения. По мере роста плотности дислокаций при холодной деформации растёт неравномерность их распределения, приводящая к концентрации напряжений в местах сгущения дислокаций и зарождению здесь очагов разрушения — трещин. В реальных кристаллах такие концентрации напряжений имеются и в исходном недеформированном состоянии (скопление примесей, частицы др. фаз и т.п.). Но вследствие пластичности металлов деформация вблизи опасных мест снимает напряжения и предотвращает разрушение. Однако, если сопротивление движению дислокаций растет, то релаксационная способность материала падает, что под нагрузкой приводит к развитию трещин (хрупкое разрушение). Это особенно проявляется в металлах с объёмноцентрированной решёткой, в которых подвижность дислокаций резко уменьшается при понижении температуры (из-за взаимодействия с примесями и уменьшения числа кристаллографич. возможных плоскостей скольжения). Предотвращение хладноломкости — одна из важнейших технических проблем разработки конструкционных металлических материалов. Др. актуальная проблема — увеличение прочности и сопротивления деформации при высоких температурах. Зародышами разрушения в этих условиях служат микропоры, образующиеся в результате скопления вакансий. Эффективный способ повышения высокотемпературной прочности — уменьшение диффузионной подвижности точечных дефектов, в частности легированием.
Применяемые в технике конструкционные металлические материалы являются поликристаллическими. Их механические свойства практически изотропны и могут существенно отличаться от свойств монокристаллов металлов. Межфазные границы вносят дополнительный вклад в упрочнение. С др. стороны, они могут быть местами предпочтительного разрушения (межзёренное разрушение) или деформации. Изменяя число и строение межфазных границ, форму и пространственное расположение отдельных структурных составляющих многофазных систем (поликристаллов, гетерофазных агрегатов, возникающих вследствие фазовых превращений, или искусственно полученных композиций), а также регулируя состав и дефектную структуру отдельных кристаллов, можно получить огромное разнообразие механических свойств, необходимых для практического использования металлических материалов.
А. Л. Ройтбурд.
Лит.: Френкель Я. И., Введение в теорию металлов, 2 изд., М. — Л., 1950; Бете Г., Зоммерфельд А., Электронная теория металлов, пер. с нем., М. — Л., 1938; Лифшиц И. М, Азбель М. Я., Каганов М. И., Электронная теория металлов, М., 1971; Абрикосов А. А., Введение в теорию нормальных металлов, М., 1972; Слэтер Дж., Диэлектрики, полупроводники, металлы, пер. с англ., М., 1969; Шульце Г., Металлофизика, пер. с нем., М., 1971.
Металлы в технике. Благодаря таким свойствам, как прочность, твёрдость, пластичность, коррозионная стойкость, жаропрочность, высокая электрическая проводимость и многое др., металлы играют громадную роль в современной технике, причём число металлов, находящих применение, постоянно растет. Характерно, что до начала 20 в. многие важнейшие металлы — Al, V, W, Mo, Ti, U, Zr и др. — либо не производились вообще, либо выпускались в очень ограниченных масштабах; такие металлы, как Be, Nb, Ta, начали сравнительно широко использоваться лишь накануне 2-й мировой войны 1939—45. В 70-х гг. 20 в. в промышленности применяются практически все металлы, встречающиеся в природе.
Все металлы и образованные из них сплавы делят на чёрные (к ним относят железо и сплавы на его основе; на их долю приходится около 95% производимой в мире металлопродукции) и цветные, или, точнее, нежелезные (все остальные металлы и сплавы). Большое число нежелезных металлов и широкий диапазон их свойств не позволяют классифицировать их по какому-либо единому признаку. В технике принята условная классификация, по которой эти металлы разделены на несколько групп по различным признакам (физическим и химическим свойствам, характеру залегания в земной коре), специфичным для той или иной группы: лёгкие металлы (например, Al, Mg), тяжёлые металлы (Cu, Pb и др.), тугоплавкие металлы (W, Mo и др.), благородные металлы (Au, Pt и др.), рассеянные металлы (Ga, In, TI), редкоземельные металлы (Sc, Y, La и лантаноиды, см. Редкоземельные элементы), радиоактивные металлы (Ra, U и др.). Металлы, которые производят и используют в ограниченных масштабах, называются редкими металлами. К ним относят все рассеянные, редкоземельные и радиоактивные металлы, большую часть тугоплавких и некоторые лёгкие металлы.
Большая способность металлов к образованию многочисленных соединений разного типа, к различным фазовым превращениям создаёт благоприятные условия для получения разнообразных сплавов, характеризующихся требуемым сочетанием полезных свойств. Число используемых в технике сплавов превысило уже 10 тыс. Значение сплавов как конструкционных материалов, электротехнических материалов, материалов с особыми физическими свойствами (см. Прецизионные сплавы) непрерывно возрастает. В то же время в связи с развитием полупроводниковой и ядерной техники расширяется производство ряда особо чистых металлов (чистотой например, 99,9999% и выше).
Применение того или иного металла (или сплава) в значительной мере определяется практической ценностью его свойств; однако существенное значение имеют и др. обстоятельства, в первую очередь природные запасы металла, доступность и рентабельность его добычи. Из наиболее ценных и важных для современной техники металлов лишь немногие содержатся в земной коре в больших количествах: Al (8,8%), Fe (4,65%) Mg (2,1%), Ti (0,63%). Природные ресурсы ряда весьма важных металлов измеряются сотыми долями процента (например, Cu, Mn, Cr, V, Zr) и даже тысячными долями (например, Zn, Sn, Pb, Ni, Co, Nb). Некоторые ценные металлы присутствуют в земной коре в ещё меньших количествах. Так, содержание урана — важнейшего источника ядерной энергии — оценивается в 0,0003%, вольфрама, являющегося основой твёрдых сплавов, — 0,0001% и т.д. Особенно бедна природа благородными и т. н. редкими металлами.
Многообразие металлов предопределяет большое число способов их получения и обработки (см. Металлургия). Взаимосвязь состава, строения и свойств металлов и сплавов, а также закономерности их изменения в результате теплового, химического или механического воздействия изучает металловедение. О свойствах, способах получения, масштабах производства и применении отдельных металлов см. в статьях, посвященных соответствующим химическим элементам и сплавам на их основе (например, Алюминий, Алюминиевые сплавы, Бериллий, Бериллиевые сплавы и т.д.).
О применении металлов и их сплавов в искусстве см. в статьях Бронза, Железо, Золото, Медь, Олово, Серебро, Сталь, Чугун, Гравирование, Гравюра, Зернь, Ковка, Насечка, Тиснение, Филигрань, Чеканка, Ювелирное искусство.
И. И. Новиков.
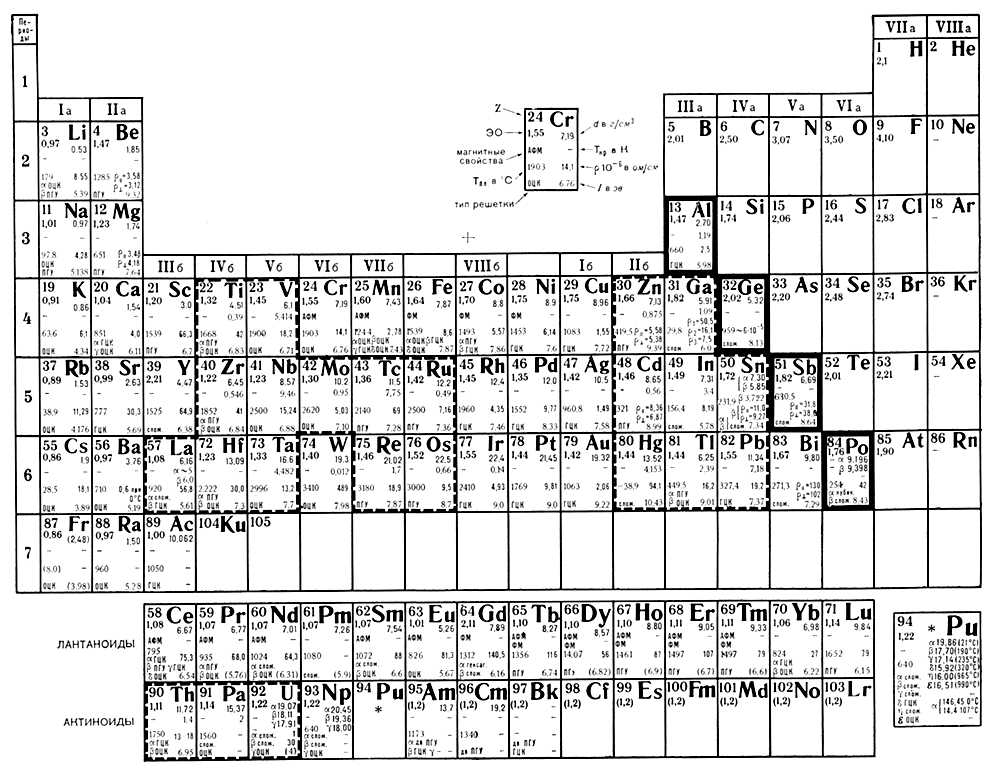
Периодическая система Д. И. Менделеева. Свойства металлов.
